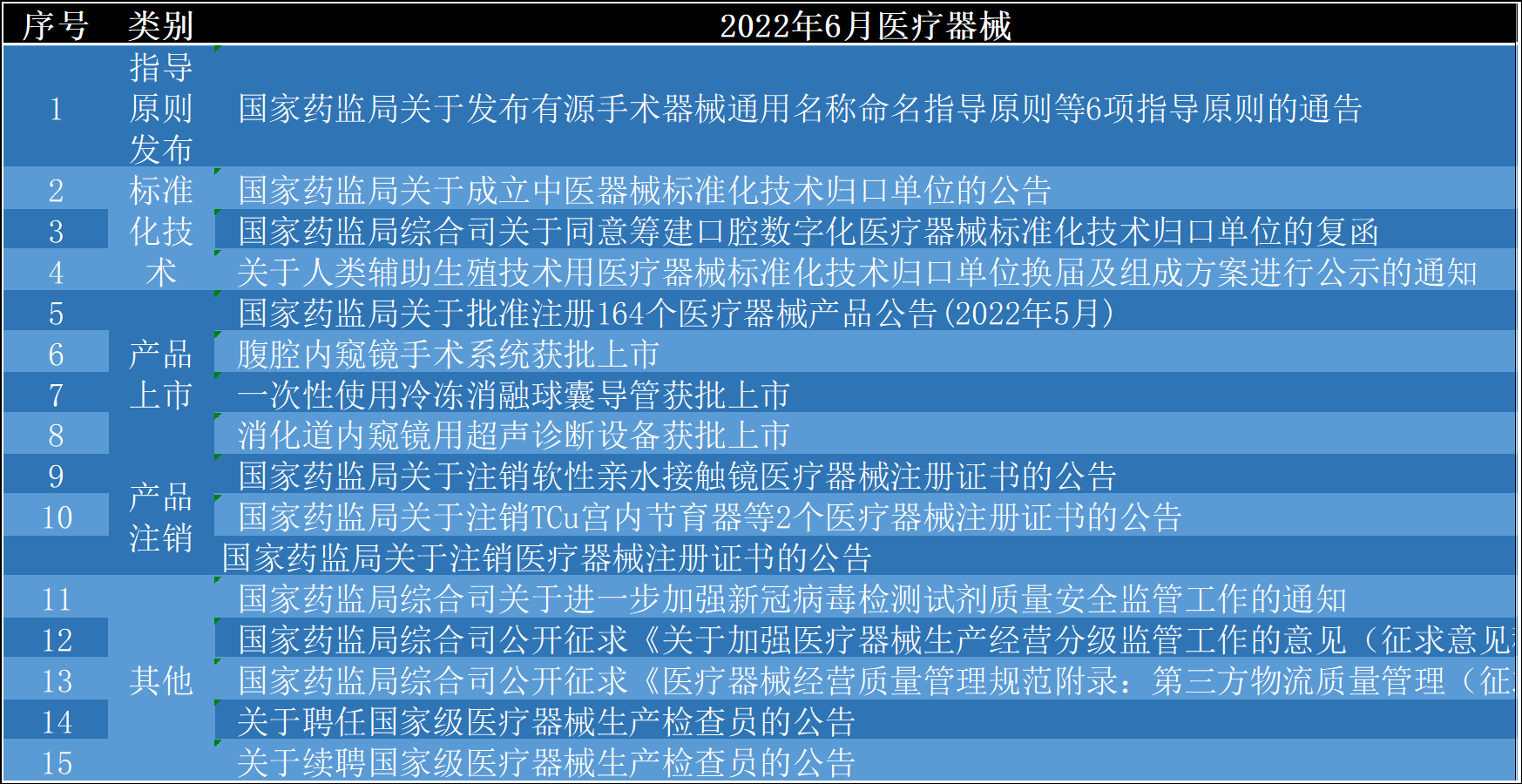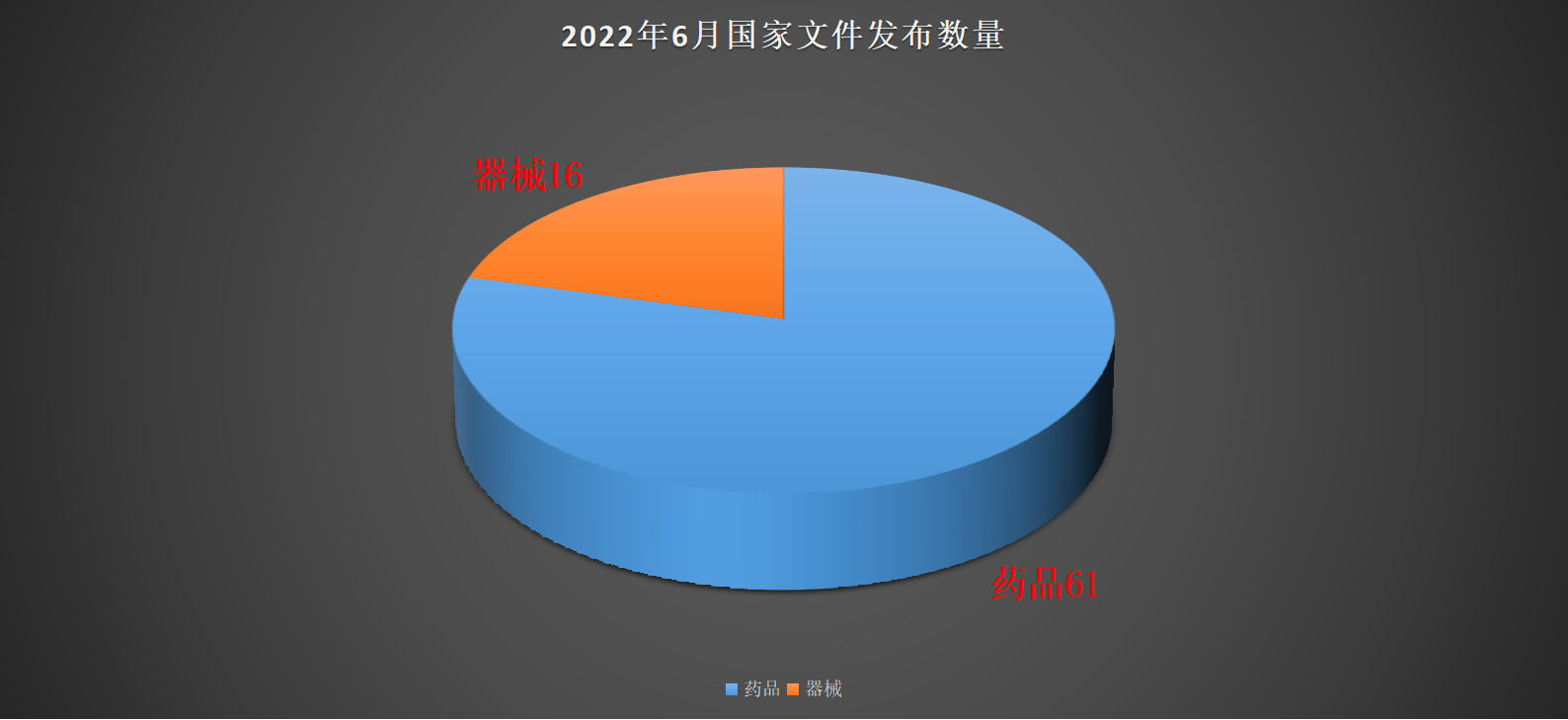
一、本月器械法规情况
本月医疗器械国家文件包括产品上市情况、产品注销情况、标准化技术归口事项、指导原则发布情况及其他事项:
1、产品上市情况:
2、产品注销情况:
2022年6月,国家局共注销5家企业9个产品医疗器械证书:
3、标准化技术归口事项:
4、指导原则发布情况:
2022年6月2日,国家局发布了6个关于器械通用名称命名的指导原则:
5、其他事项:
二、本月药品法规情况
1、国家局陆续公布2021年审批战报
2、儿童用药目前备受国家关注
3、国家局发布最新药包材相关规范和指导原则
4、中药方面涉及中药配方颗粒和中药标准事宜
5、电子化的未来已到,中检院更换新章

6、6月多个指导原则公布
6.1.征求意见指导原则:
6.2.试行指导原则:
7、最迟明年药品追溯系统将覆盖所有药品
8、国家统一修订氨糖美辛制剂说明书安全事项
9、支持港澳药品、器械企业来大湾区内地9市发展
10、产品上市
2022年6月29日,国家局公布三家企业三个产品上市,其中1类创新药2个,国内2个产品是通过优先审评审批程序附条件批准上市:
11、其他(国家药监局研究推进加入PIC/S工作)
三、本月法规清单