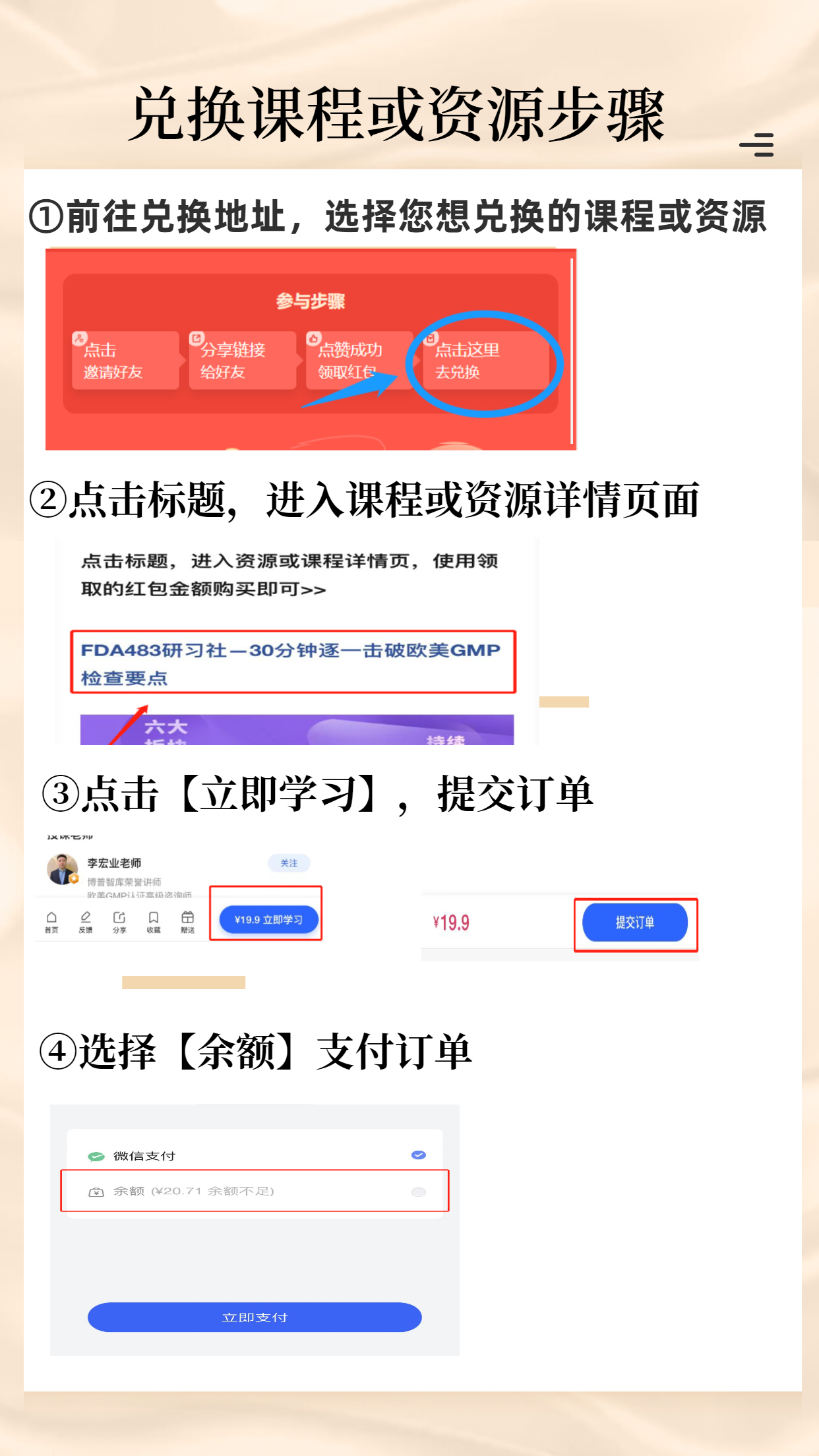
点击领取学习红包兑换课程及资源>>>
生物药发展研究分析及下游工艺开发

FDA483研习社—30分钟逐一击破欧美GMP检查要点

制药企业如何迎检

药品注册现场检查要点及实例分析

图说质控—第一期

2、药品注册核查课程

其它付费课程:
点击【智库学院】
质量管理体系培训-21节课
GMP基础知识学堂
药品注册现场检查要点及实例分析
CSV&DI晋升必修—药企数字化实战经验分享
从法规到应用,掌握CSV正确方法
FDA483研习社—30分钟逐一击破欧美GMP检查要点
四个统计学分析技巧,解决年度质量回顾分析难题
质量负责人教您如何制定明年质量目标
年度回顾中的偏差分析
从法规到应用,掌握物料风险评估的正确方法
年度质量回顾-统计学干货-从基础概念到案例实操全面剖析
GMP基础课程
年度质量回顾中稳定性试验考察的要求和检查实践
专业资源:
《ISPE-Good Practice Guide_Practical Implementa
ISPE记录和数据可靠性指导原则.(RDI)
《ISPE Baseline Guide Vol 3 Sterile Product Manufacturing》
《ISPE GAMP Good Practice Guide Enabling Innovation-2021》
《ISPE GAMP Good Practice Guide Computerized GCP Systems and data》
《ISPE记录和数据可靠性指导原则》
《ISPE GAMP Good Practice Guide Calibration Management
《ISPE 良好做法指南:维护第2版 GPG Maintenance 2nd 2021
《ISPE良好实践指南:制药行业的知识管理》
《ISPE APQ 指南:管理职责和审查上市后变更政府法规汇总数据完整性法规梳理思维导图ISPE记录和数据可靠性指导原则PDA TR 60-3 工艺验证 - 生命周期方法新药注册申报资药品注册法规汇编全集GAMP IT InfrastructurePDA TR 48-2010PDA TR 66 2014 原版PDA TR 69 Bioburden and Biofilm ManagementPDA TR51 Biological Indicators for Gas and Vapor《ISPE良好实践指南:制药行业的知识管理》ISPE APQ 指南:管理职责和审查ISPE GAMP Good Practice Guide Enabling Innovation-2021药品上市许可持有人制度(MAH)法规汇编全集常用药物辅料手册药物临床试验机构管理制度 上册 临床试验机构管理制度与SOP好书--药物化学总论(第4版)ICH-M7(step4)基因毒性杂质评估和控制◆中英药品注册法规手册(第3版)2021.12.31研发管理WHO指南-段段对照
美国新药申报指南
ISPE Good Practice Guide Biopharmaceutical Process Developme
ISPE Baseline Guide Vol 3
液相色谱手册——液相色谱柱与方法开发指南
制药配液风险控制相关技术考虑要点(张伟,董江萍编者)
【干货资料合集】
分析方法验证指南汇总
全套GMP文件
欧盟GMP指南及法规资料收录
ISPE相关法规及指南收录
CDE药品技术评价文集(全册)
药品注册员成长指南(法规、培训)
QC实验室管理资料
WHO各类指南文件合集
点击【智库资源】搜索,查看更多!

