2022年5月9日,中华人民共和国药品管理法实施条例征求意见在行业人事的期盼中,终于出炉。
自2019年8月26日中华人民共和国药品管理法修订通过,并予以发布,到2019年12月1日施行。再到2022年5月9日发布,共历时2年零8个月。
以下是个人学习的思路总结给大家分享:
在学习法律法规的时候,你是否有看完后脑子中没印象、看完不知里面说打什么东西,那么恭喜你,这说明你还是一个小白,面对小白,我们如何快速了解一篇法律法规呢,下面我们通过学习药品管理法实施条例
面对新发布的实施条例
作为生产企业人员来说,学习药品管理法实施条例可以分为四个阶段:第一阶段:掌握第三、四章;第二阶段:熟悉第二、九章;第三阶段:了解第一、八章;第四阶段:拓展其他章节;
这样以来,你才能学到对自己最有用的知识,拓展其他相关知识。
第一阶段:药品上市许可持有人、药品生产(三、四章节)
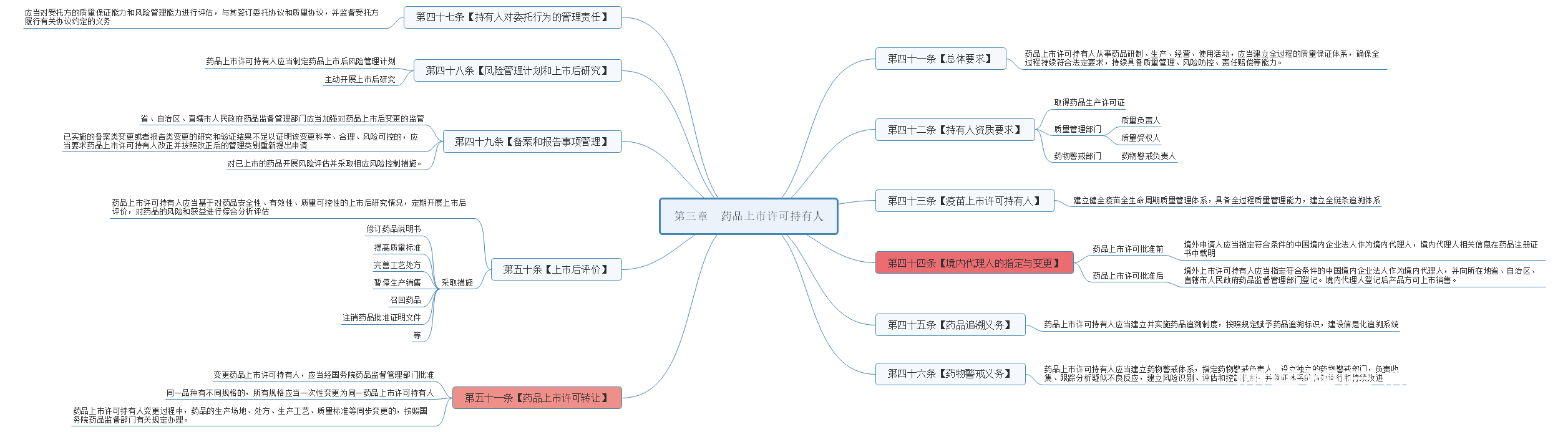
【总体要求】、、
看来目录大家应该就比较清场,这一章节主要讲述的内容了,再次,我就不一 一 说明了,导图中也列出了关键点,大家可以自行学习。后续内容我只列出目录,仅供大家熟悉。

药品管理法实施条例【生产许可】、【生产许可证载明事项】【生产许可期限】【人员管理要求】【生产管理要求】【物料管理要求】【持有人对委托生产的管理】【境外生产要求】【注册前规模批药品上市销售】【疫苗委托生产】【疫苗生产要求】【中药材管理】【中药材产地加工】【中药材包装标签】【中药饮片生产管理】【中药饮片包装标签】【中药配方颗粒管理】【分段生产管理】。
第二阶段:药品研制与注册、法律责任(二、九章节)
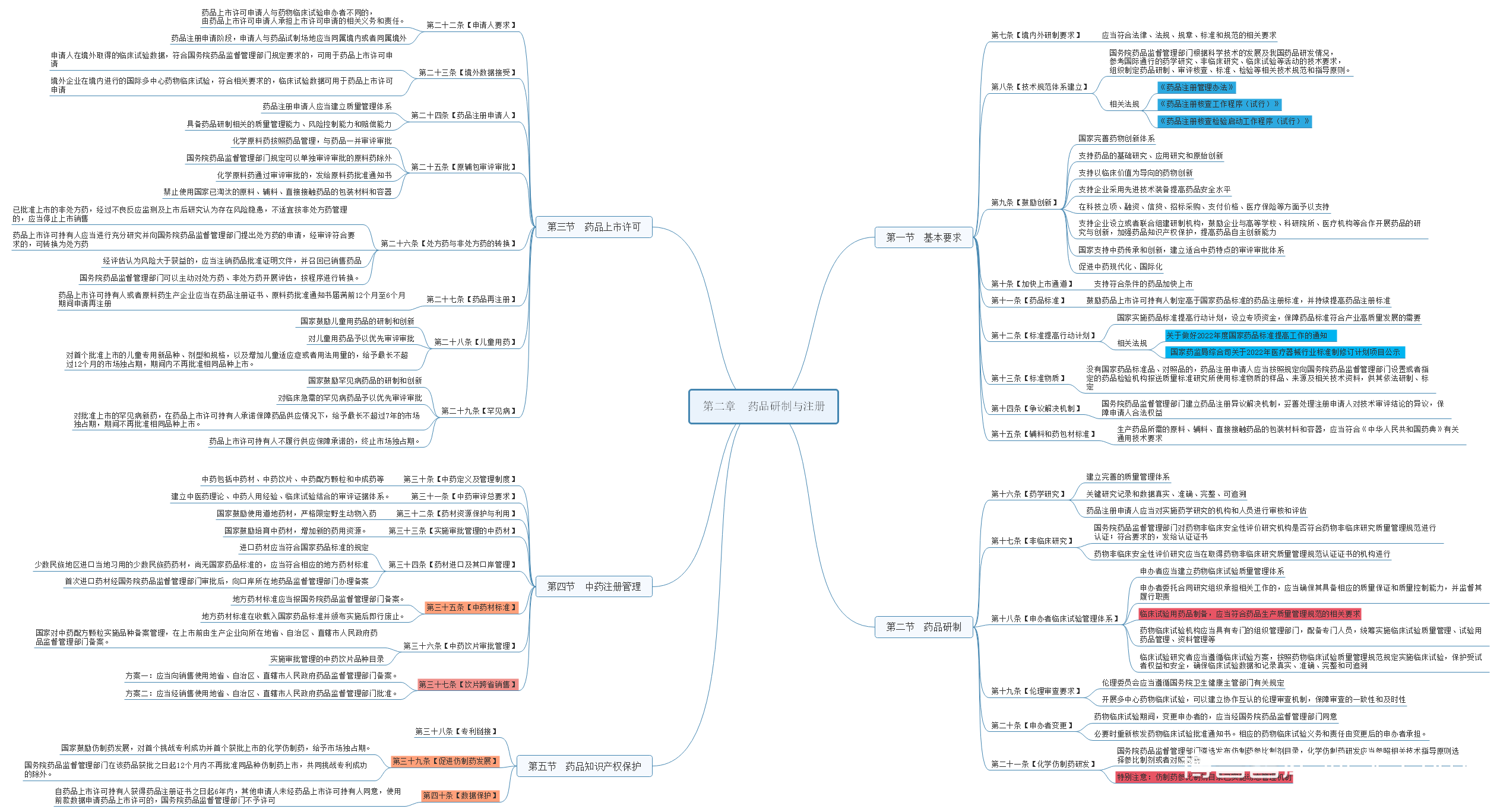
第一节基本要求:【境内外研制要求】【技术规范体系建立】【鼓励创新】【加快上市通道】【药品标准】【标准提高行动计划】【标准物质】【争议解决机制】【辅料和药包材标准】第二节药品研制:【药学研究】【非临床研究】【申办者临床试验管理体系】【伦理审查要求】【申办者变更】【化学仿制药研发】第三节药品上市许可:【申请人要求】【境外数据接受】【药品注册申请人】【原辅包审评审批】【处方药与非处方药的转换】【药品再注册】【儿童用药】【罕见病】第四节中药注册管理:【中药定义及管理制度】【中药审评总要求】【药材资源保护与利用】【实施审批管理的中药材】【药材进口及其口岸管理】【中药材标准】【中药饮片审批管理】【饮片跨省销售】第五节药品知识产权保护:【专利链接】【促进仿制药发展】【数据保护】
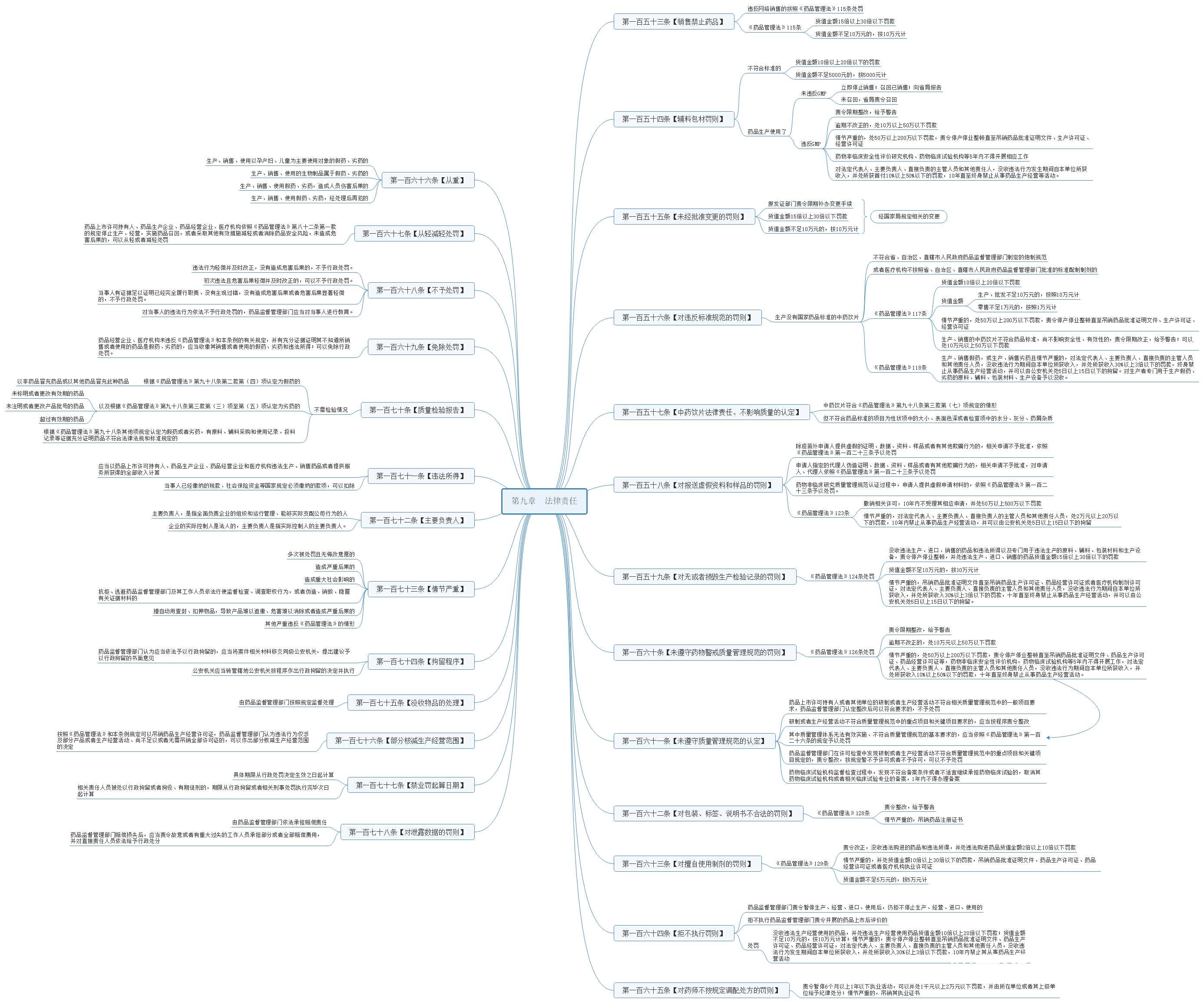
【销售禁止药品】【辅料包材罚则】【的罚则】【对违反标准规范的罚则】【中药饮片法律责任、不影响质量的认定】【对报送虚假资料和样品的罚则】【对无或者损毁生产检验记录的罚则】【未遵守药物警戒质量管理规范的罚则】【未遵守质量管理规范的认定】【对包装、标签、说明书不合法的罚则】【对擅自使用制剂的罚则】【拒不执行罚则】【对药师不按规定调配处方的罚则】【从重】【从轻减轻处罚】【不予处罚】【免除处罚】【质量检验报告】【违法所得】【主要负责人】【情节严重】【拘留程序】【没收物品的处理】【部分核减生产经营范围】【禁业罚起算日期】【对泄露数据的罚则】
第三阶段:总则、监督管理(一、八章节)
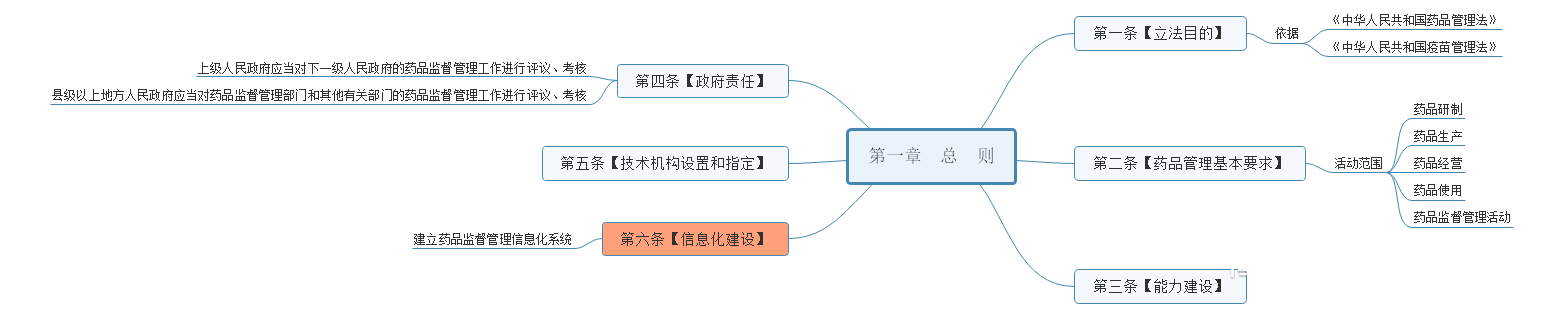

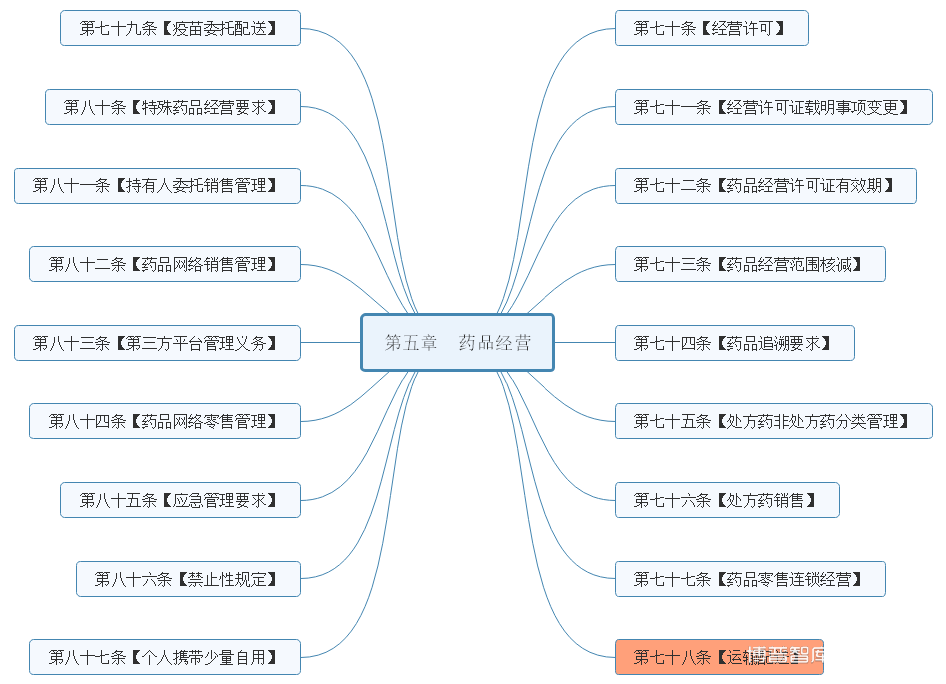
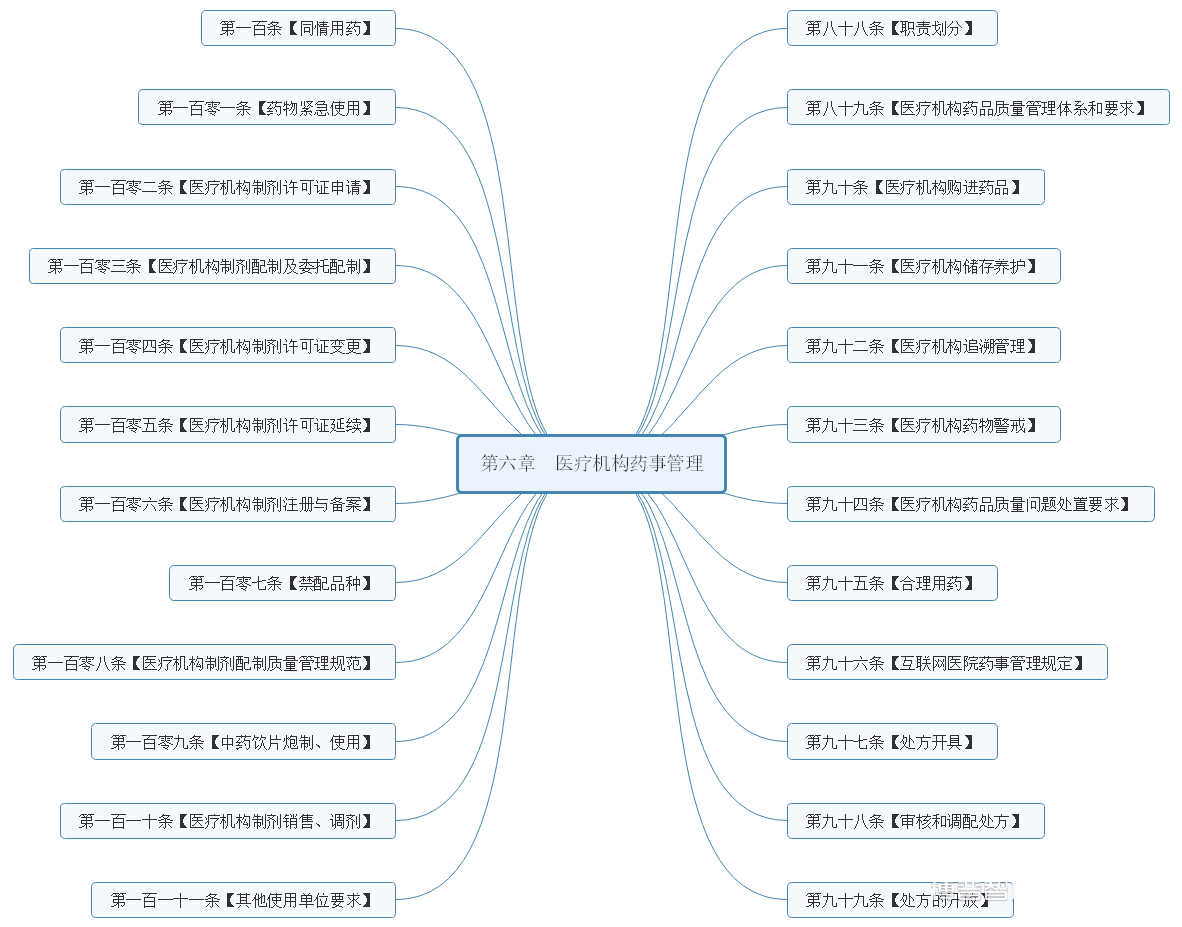
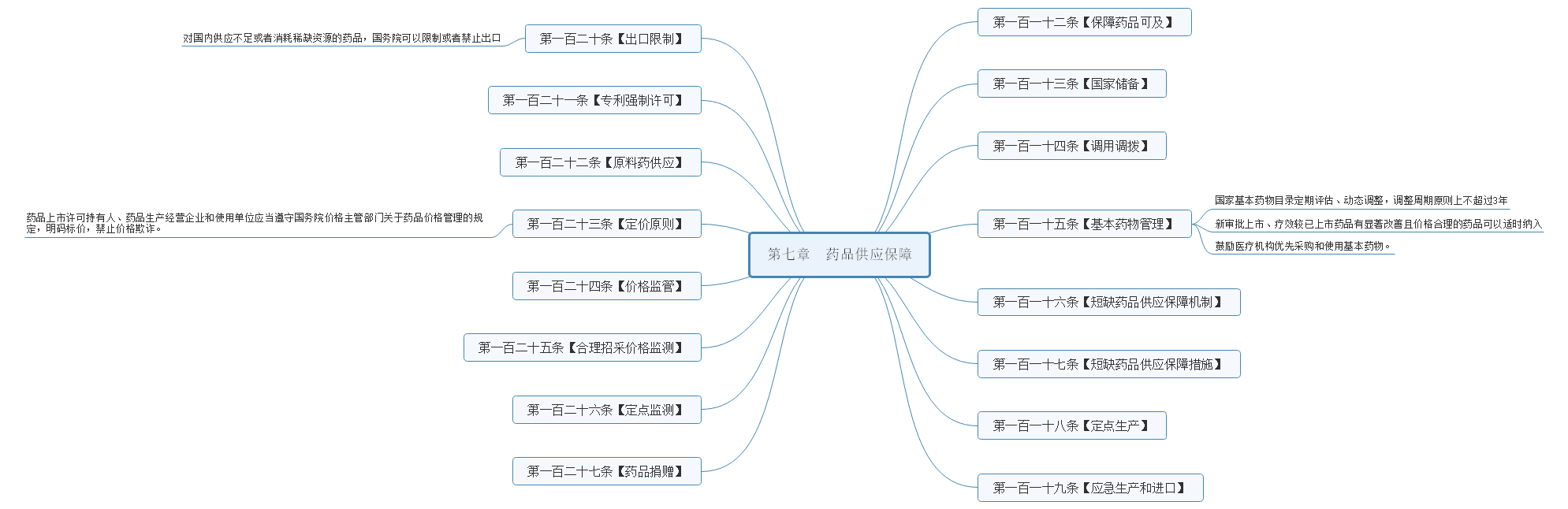
对于工作来说,药品管理法实施条例有学习主次之分;但对于个人来说,章节就没有主次之分,想要提高,就得分清楚先学哪些部分,后续在学哪些部分,而不是说哪些学,哪些不学关注我,待药品管理法实施条例正式稿实施后,可以及时了解正式稿发生哪些变化!

