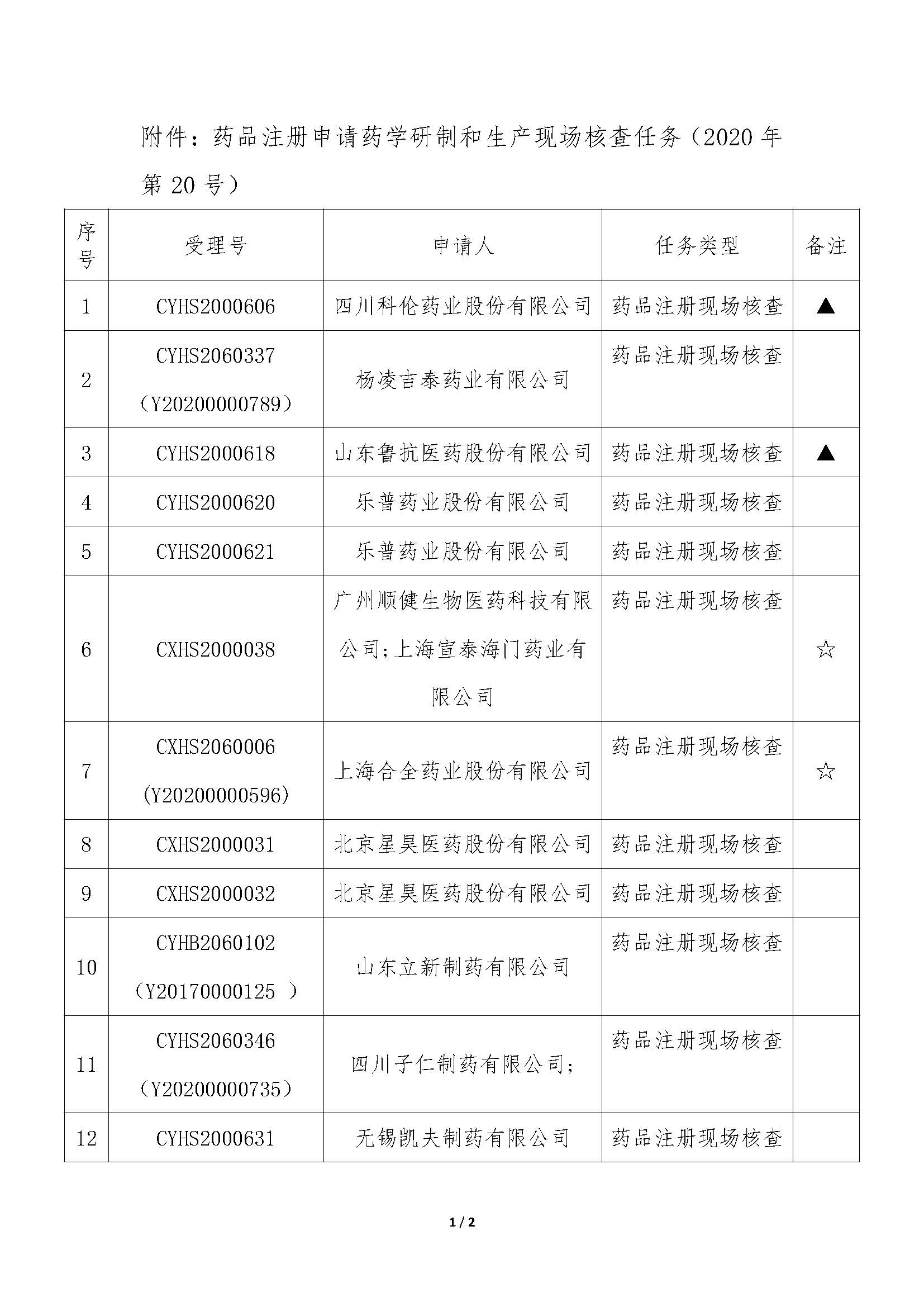
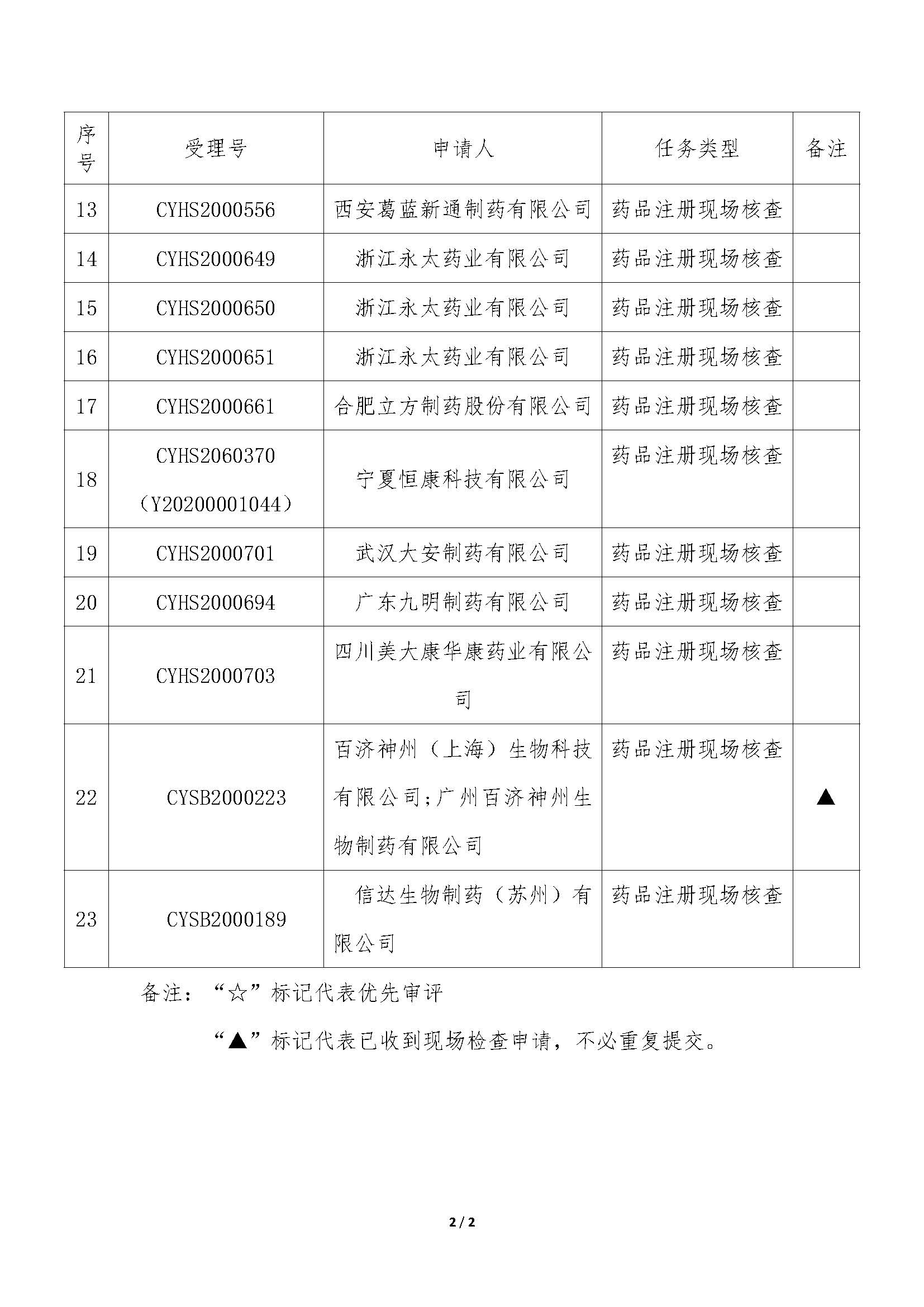
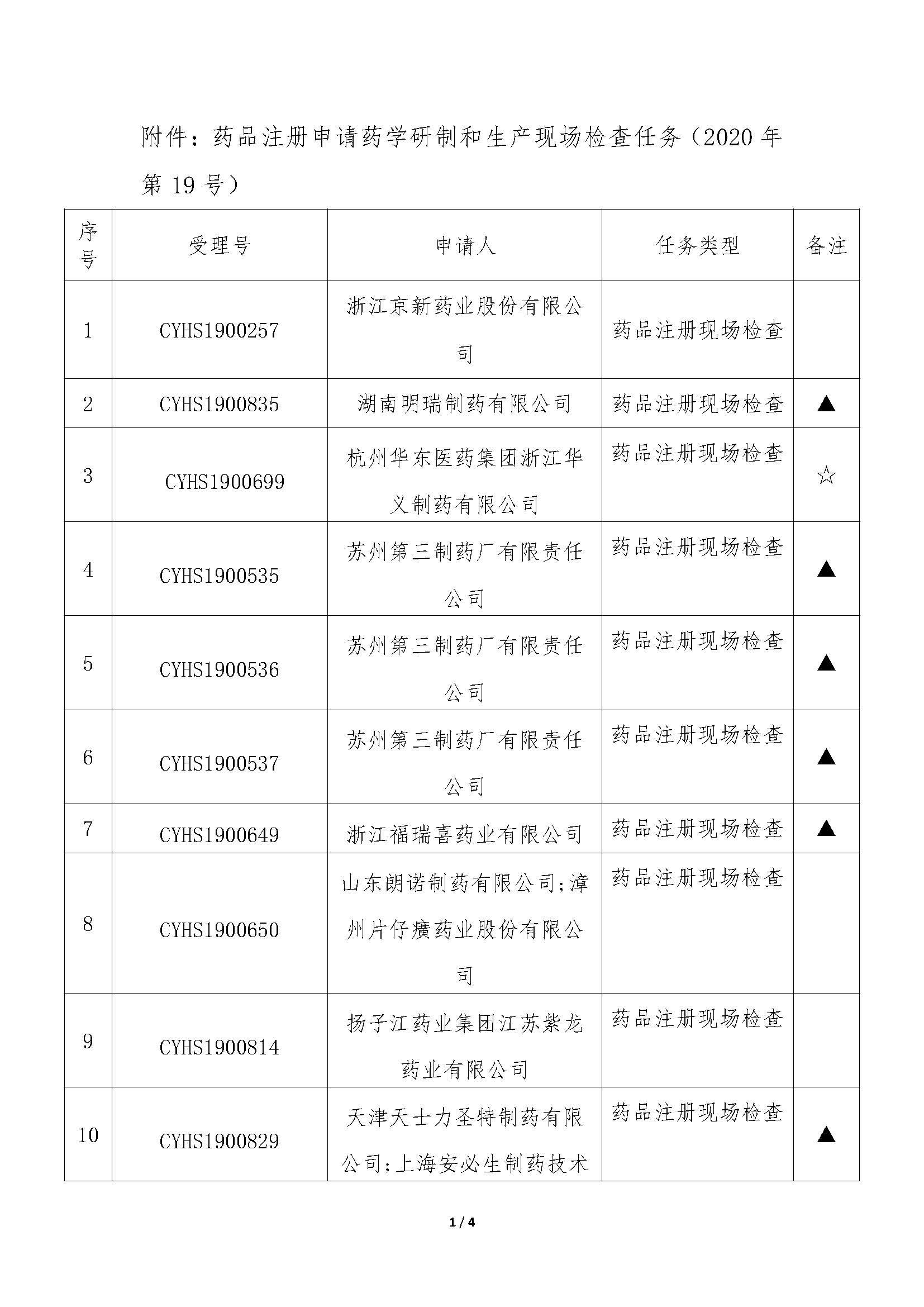
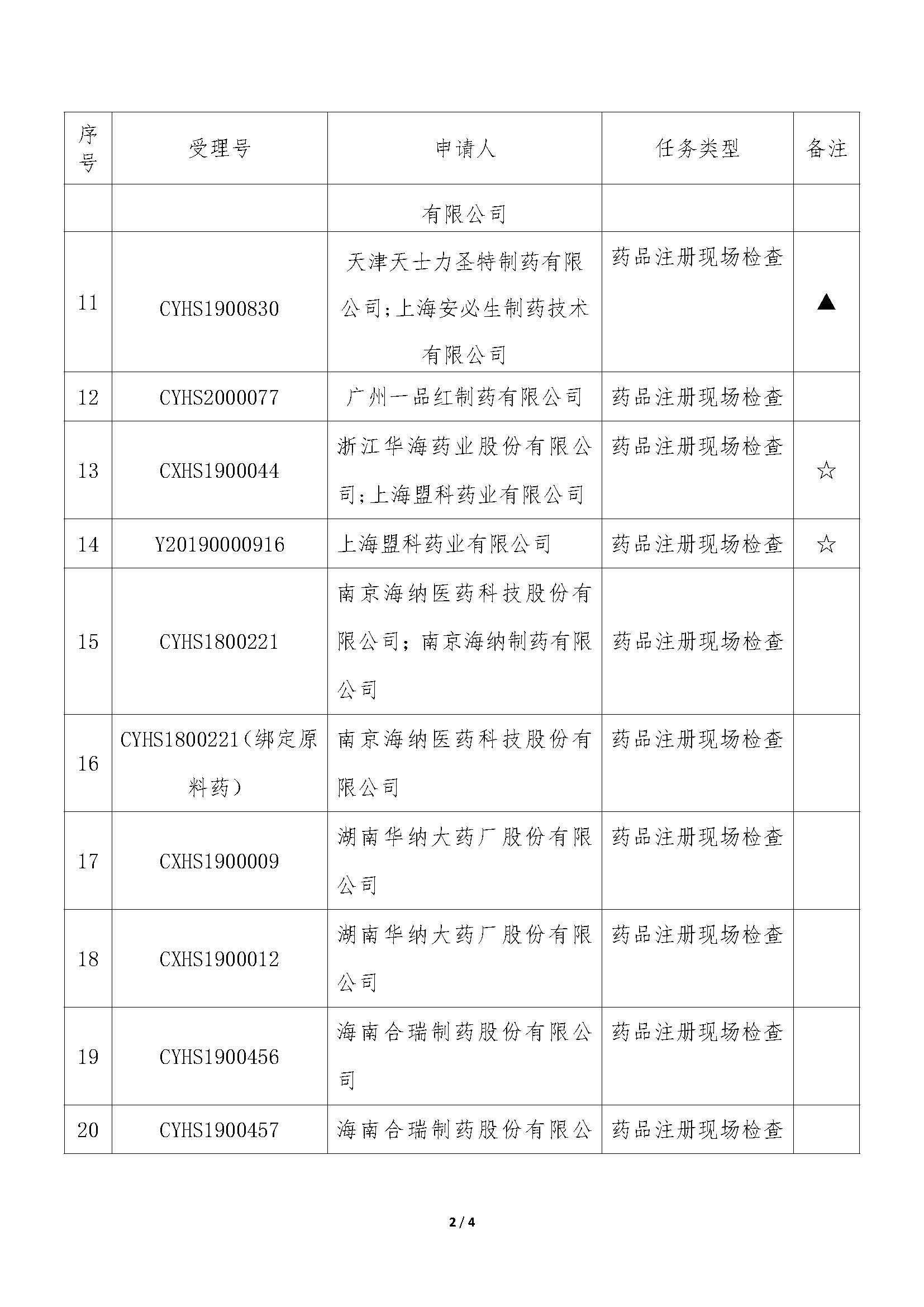
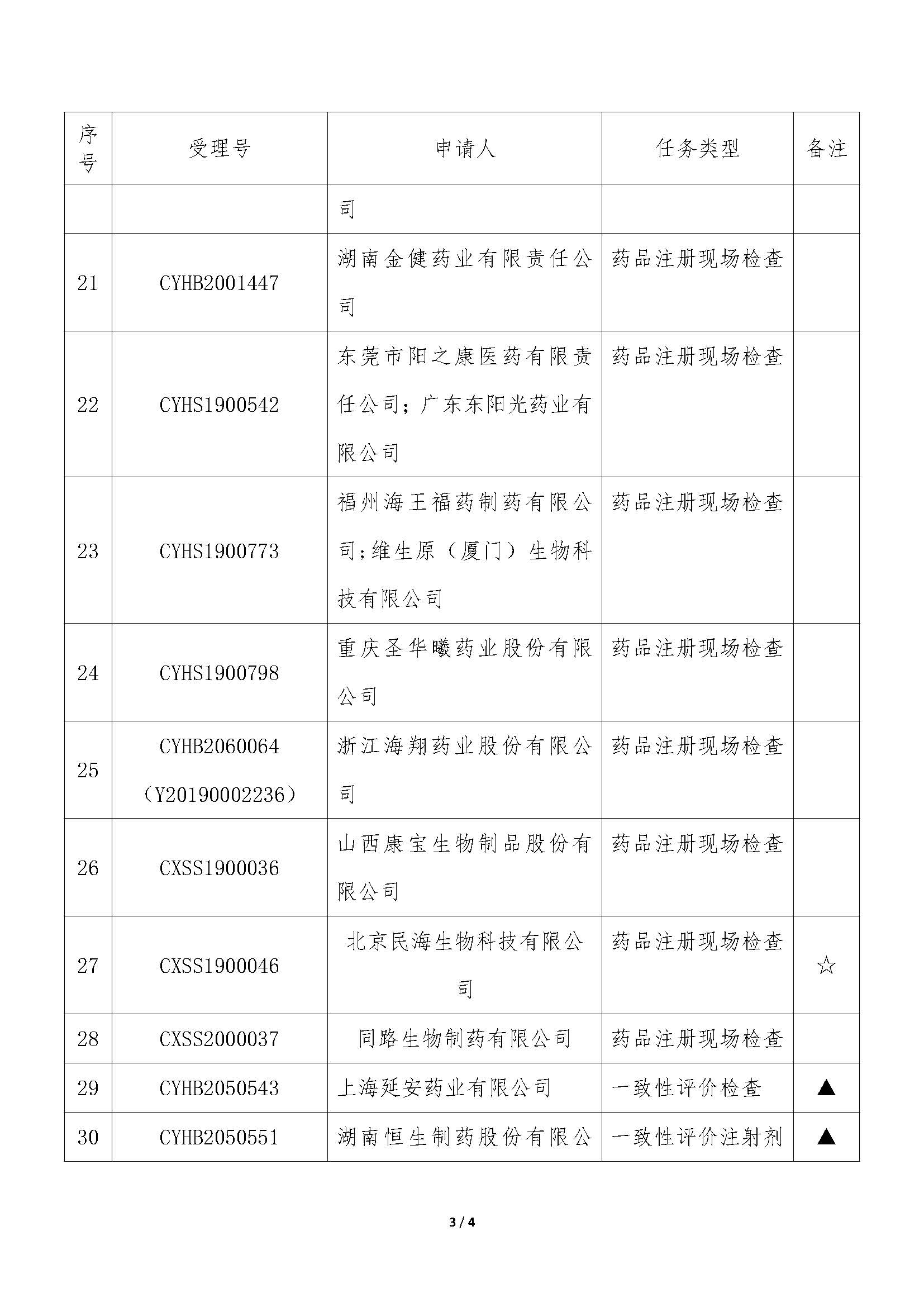
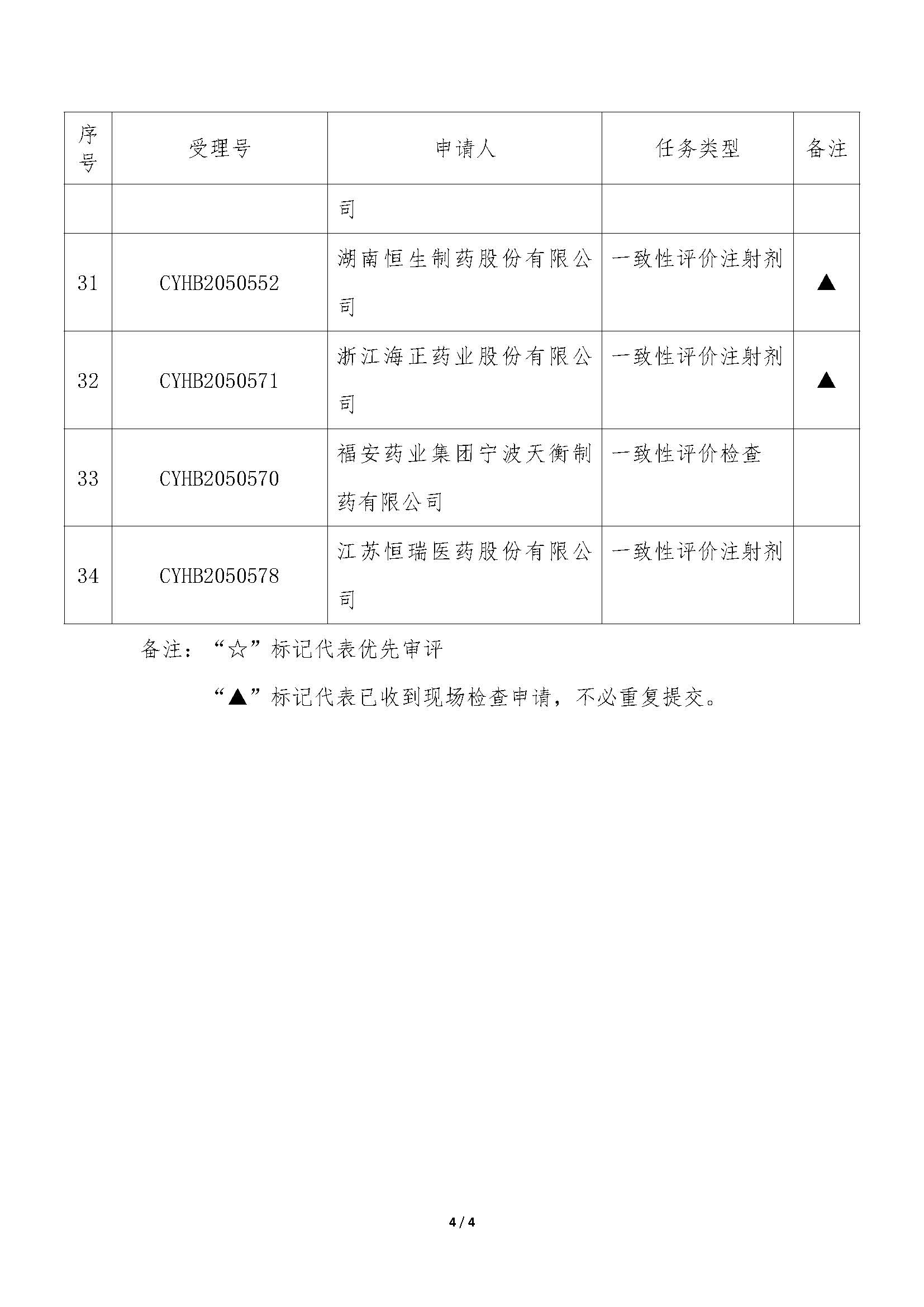
今日,国家药品监督管理局食品药品审核查验中心发布2条公告,【药品注册申请药学研制和生产现场检查任务信息公告】(2020年第19号)(2020年第20号),本次公布的检查任务主要是:34个药品注册申请的药学研制和生产现场检查任务(其中28个药品注册现场检查,所占比例为82.4%,其他6个为一致性评价检查相关),以及23个药品注册申请的药学研制和生产现场核查任务。

我中心已接收药品审评中心发起《药品注册管理办法》(市场监管总局令第27号)实施前受理的34个药品注册申请的药学研制和生产现场检查任务,相关任务信息现予以公告(详见附件)。
根据原《药品注册管理办法》(国家食品药品监督管理局局令第28号),已接收到药品审评中心相关申请生产现场检查通知文件的注册申请人,且自认为具备接受现场核查条件的,需在规定时间内登陆我中心网站(www.cfdi.org.cn( www.cfdi.org.cn)
www.cfdi.org.cn)
请相关药品注册申请人予以关注,逾期不提交,我中心将按照有关规定终结相关检查任务,并回复药品审评中心。
感谢支持和配合。如有不解事宜,请与我中心联系。
联系人:陆德 刘瑾欣
联系电话:010-68441676 010-68441674
传 真:010-68441300
联系地址:北京市西城区文兴街1号院3号楼北矿金融大厦6层
邮 编:100044
附件:
药品注册申请药学研制和生产现场检查任务(2020年第19号).docx

我中心已接收药品审评中心根据《药品注册管理办法》(市场监管总局令第27号)第48条规定启动的第四批23个药品注册申请的药学研制和生产现场核查任务,相关任务信息现予以公告(详见附件)。
根据《药品注册管理办法》,请已收到药审中心相关药学研制、生产现场核查告知材料的注册申请人,尽快登陆我中心网站(www.cfdi.org.cn( www.cfdi.org.cn)
www.cfdi.org.cn)
请相关药品注册申请人予以关注,按照相关程序规定逾期提交者,我中心将顺延相关核查任务组织和完成时间,并通知药品审评中心。
感谢支持和配合。如有不解事宜,请与我中心联系。
联系人:陆德 刘瑾欣
联系电话:010-68441676 010-68441674
传 真:010-68441300
联系地址:北京市西城区文兴街1号院3号楼北矿金融大厦6层
邮 编:100044
国家药品监督管理局食品药品审核查验中心
2020年12月3日
附件:
药品注册申请药学研制和生产现场核查任务(2020年第20号).docx