网页端用户可点击右方目录直接跳转至制定章节
转发本文到朋友圈,添加微信pckt6842 免费领取【一致性评价法律法规目录】
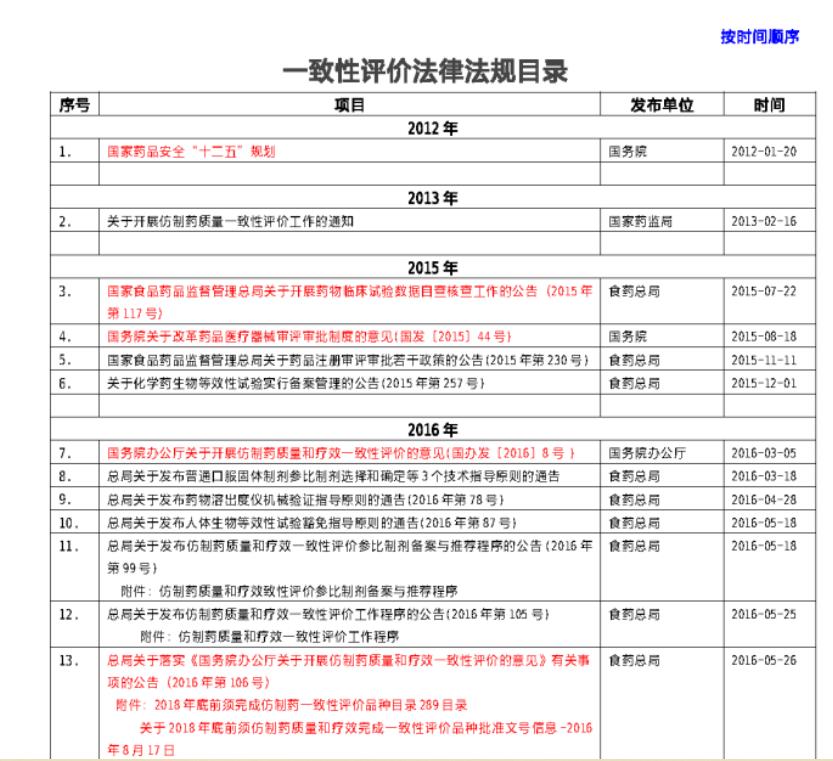
1. 概念
2012年,《国家药品安全“十二五”规划》明确提出要用5~10年时间,对2007年修订的《药品注册管理办法》实施前的仿制药,分期分批与被仿制药进行全面比对研究,使仿制药与被仿制药达到一致。
对象和时限:
(一)《国家基本药物目录(2018年版)》( 《国家基本药物目录(2018年版)》)已于2018年11月1日起施行并建立了动态调整机制 , 与一致性评价实现联动。通过一致性评价的品种优先纳入目录,未通过一致性评价的品种将逐步被调出目录。对纳入国家基本药物目录的品种 , 不再统一设置评价时限要求。
《国家基本药物目录(2018年版)》)已于2018年11月1日起施行并建立了动态调整机制 , 与一致性评价实现联动。通过一致性评价的品种优先纳入目录,未通过一致性评价的品种将逐步被调出目录。对纳入国家基本药物目录的品种 , 不再统一设置评价时限要求。
(二)化学药品新注册分类实施前批准上市的含基本药物品种在内的仿制药,自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价。逾期未完成的,企业经评估认为属于临床必需、市场短缺品种的,可向所在地省级药品监管部门提出延期评价申请,经省级药品监管部门会同卫生行政部门组织研究认定后,可予适当延期。逾期再未完成的 , 不予再注册。详见 2018年第102号 公告( 详见 2018年第102号 公告)
详见 2018年第102号 公告)
2. 法规指南
CDE官方 仿制药一致性评价专栏
3. 资源推荐
3.1 优质专栏
仿制药一致性评价文章合集
一致性评价资料收集(培训\经验总结)
仿制药一致性评价相关指导文件分享
3.2 优质文章
3.3 优质课程





