5.2.7
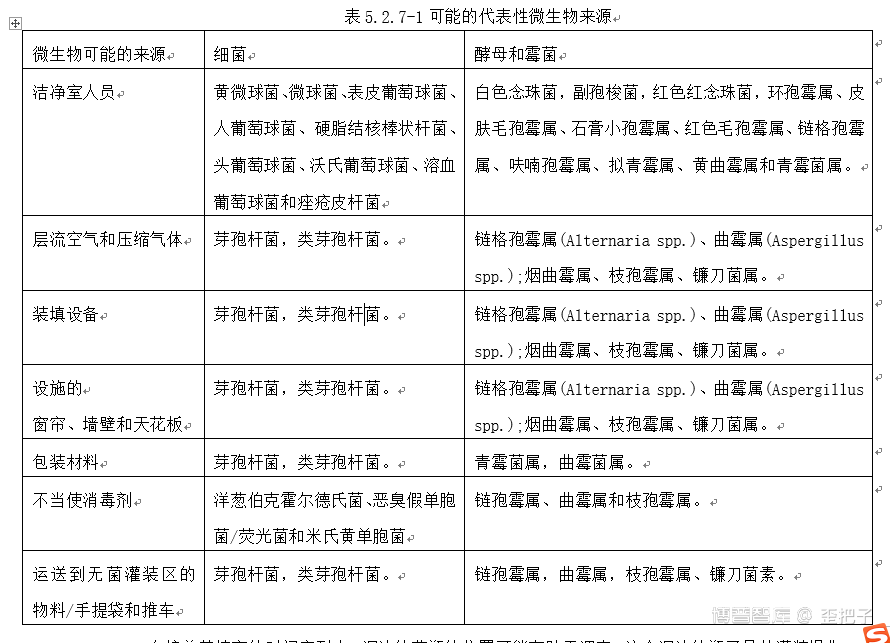
从浑浊瓶中分离出的微生物可能来自洁净室人员、设备表面、墙壁和天花板、地漏、包装材料、消毒剂或运输到无菌灌装区的材料。它们可能对应于EM和产品无菌检测中分离的微生物。表5.2.7-1包含一个有代表性的微生物样本,根据工作队成员的经验,在失败的培养基灌装中发现了这些微生物及其可能的来源。这些微生物以最近的一篇关于洁净室微生物的综述为基准【40】。
在培养基填充的时间序列中,浑浊的药瓶的位置可能有助于调查。这个浑浊的瓶子是从灌装操作的开始,中间,还是结束?从灌装开始的浑浊瓶可能是在灌装站无菌装配灌装活塞或针头期间微生物污染的结果;从灌装的中间,它可能与操作员的干预有关,如清理下瓶的输送带,进行定期的灌装体积检查,或补充塞料斗;从灌装结束开始,可能与不良的无菌操作或操作疲劳有关。如果灌装单元按顺序编号或打上时间戳,则可以查看培养基灌装的视频,并确定是否发生了事件或干预,以及单个培养基灌装瓶何时被污染。如果培养基填充不能被录像,观察者应该记录所有发生的事件和干预,以帮助调查或改善洁净室实践。
5.2.8
如果最初的实验室调查(第4.0节)没有发现解释偏差的实验室误差的决定性来源,则应检查与制药用水系统相关的偏差。
水在制药生产中有许多用途,所需的水等级因其使用方式而异。汇编定义了每一水等级必须满足的最低质量属性,并详述了其制备方法。制药用水系统由几个部分组成,包括原水供水系统、可靠的净化系统,该系统应在一系列条件下持续生产出预期质量的水,储存和分配系统,确保水在被输送到生产过程之前继续满足所有要求的质量属性。总之,水系统的设计、安装和确认,以及其操作、使用和维护的程序,确保系统始终如一地按照预期和控制状态运行。
负责调查与水系统相关的任何偏差的跨职能团队应该熟悉与设计、安装、操作、使用和维护相关的潜在风险。这个团队还需要了解从系统确认和监视中获得的数据的价值和局限性。
监测计划应定义取样的位置、频率和检测的属性。该计划应包括整个系统,从供水到使用点,以及在制备、储存和分配系统之间的相关点。取样计划应反映确认期间的密集取样结果、最近的历史数据、风险因素和缓解措施。应仔细选择监测点,以确保它们提供有关系统控制的预期资料,包括支持对该点或系统上其他点的偏差进行初步调查所需的资料。
对水的生产、储存和分配系统的例行监测可以核实它们是否继续在控制状态下运行,而对用水点的监测则可以评估输送到该工序的水的质量。使用点应定期取样和检测(通常离线)化学属性。在进行偏差调查时,这些化学测量可以作为有用的参考。在制备单元操作之前和之后进行的测量,如活性炭罐、阴阳离子柱、紫外线灯和反渗透系统,可以提供数据来评估它们是否继续按预期运行。
微生物监测通常包括从储罐、循环上的点或使用点手工采集样本;样品的运输、储存和分析;最后,记录、解释和报告结果。每一步都应仔细设计,以尽量减少潜在的误差,并确保报告的结果准确地反映取样材料的情况。此外,有若干监测系统可用于微生物属性的在线监测,与其他取样和测量关键属性的仪器一样,这些监测系统应经过适当的确认。有关监测计划的其他指引,请参阅PDA第13号技术报告《环境监测项目基本原则》【4】。
调查制药用水系统偏差的根本原因的方法应根据样品的位置和时间以及所涉及的测试来指导。如果观察到同一类型、同一水平的多个偏差,则更有可能是影响整个系统的原因。如果偏差与其他同期样品的结果不一致,可能会怀疑与取样点或取样或测试有关的原因。每个水系统的偏差都是独特的,其调查可能会考虑与系统的设计、安装、运行、维护、变更历史和使用相关的因素。监测历史,包括偏差调查、相关capa和系统典型微生物谱系,将提供有用的参考。
在生物负荷偏离的情况下,回收的生物体鉴定将提供必要的信息。在水中良好成长并形成生物膜的生物体的回收可能意味着一组原因,而与水系统不相容的生物体的回收可能意味着另一组原因,如,可能与环境污染有关。
饮用水是纯化水和WFI的起始物料。由地区当局制定的标准至少要求饮用水不含大肠菌群和含有指定水平的生物负荷(例如,依据USP-1231,500CFU/mL),它们可能还规定了额外的要求。纯化水必须满足药典规定的电导率、总有机碳和微生物负荷(100CFU/mL)限值。WFI必须满足相同的物理和化学标准,以及更严格的微生物负荷标准(<10CFU/100mL)和细菌内毒素限度(<0.25EU/mL)。
饮用水的来源和输送方法可能给水系统的控制带来重大风险。饮用水质量可能受到季节性变化的影响,这是由于融雪径流或降水枯水期造成的。农业或工业径流可能进入地表水源或含水层。老化的基础设施可能会增加污染通过损坏的水管进入供水系统的机会【50】。同样,通过卡车运送水会带来各种各样的风险,这些风险可能因车的不同而每天都不同。饮用水供应的抽样和分析计划应考虑与供应来源和方法有关的风险,并应事先考虑调查饮用水供应或下游系统的样品中发现的偏差所需的信息。
与水系统的设计和安装有关的风险应该在确认测试之前确定和纠正。系统边界应该为微生物污染提供一个有效的屏障,包括在储罐上的微生物保安过滤器和使用适当的垫片密封圈等弹性体。死角,以及不良的焊接和其他不规则的表面,增加了生物膜形成的风险。最近的设计标准规定,从主循环回路分支出来的管道不应超过管径的1.5倍,现在普遍使用无死角的阀门。
偏差的调查应包括系统操作的审查,包括物理参数的控制,以及系统的非微生物监测结果。存储和分配系统的操作控制通常包括温度、流量和压力等参数,可以显示系统是否处于溢流状态或流动状态,以及是否处于所需的温度。还可以为预处理阶段(如碳床、去离子器和反渗透系统)定义其他参数。物理和化学属性的在线、在位和离线测量,如硬度、电导率和总有机碳,提供了化学属性的近距离连续数据。它们还允许对性能的意外变化进行及时通知,这有助于调查偏差。水的利用率影响水在系统中的滞留时间,可能与根本原因有关。
偏差的调查可能包括对日常和纠正性维护记录的审查。侵入性开口维护增加了污染风险,因此应该尽可能提前准备减轻这些风险和使系统恢复服务的措施。水系统维护应确保系统保持完整,并继续在控制状态下运行。一个精心设计的程序确保系统边界继续提供一个有效的屏障,防止微生物污染。应采取的措施包括定期更换关键部件,如储罐上的密封圈垫片等弹性体和排气过滤器,因为这些部件的故障会导致系统向外部环境开放。对偏差的调查还应考虑对管道等耐用部件的潜在磨损和损坏。随着时间的推移,管道可能会变薄,并可能由于意外事件(如液压冲击)而发生损坏。漏水应及时修理,减少污染机会;然而,对偏差的调查应该认识到,并不是所有的泄漏都很容易检测到,例如,通过破裂的热交换器管的冷却水的小泄漏。
应考虑样品口或使用端口的操作方法,特别是当偏差与其他结果不一致时。取样(和使用)前的冲洗是很重要的,要物理地清除在软管、取样设备或取样口上发现的机会性微生物。使用程序应确保在水系统和下游点之间使用阀门不会造成死体积。在不使用时,软管应该拆卸下来,并应储存在一个可自由排水的位置。
5.2.8.1压缩气体
在制药产品的生产和检测过程中使用的压缩气体有空气、氮气、氧气和二氧化碳。不适当的设计和分配这些气态物质的管道可能会引入不必要的微生物。药物级压缩空气被处理以去除水分,化学残留物如润滑剂,除菌级过滤器在使用点可能被应用。引入不受控制的水分或过滤不充分的压缩气体,再加上气体输送系统设计不良的预处理和卫生处理工艺,会对系统产生不利影响,导致产品污染。
用于测试这些系统中微生物存在的方法类型是重要的,因为当成品药品中发现异常时,QCU最终的调查必须找到污染源,或至少,消除了它来自压缩气体的可能性。
即使这些公用系统符合设计要求,在其施工过程中使用的材料可能含有意外的部件缺陷(例如,焊接不良或钝化不完全),以及可能会进入用于设备润滑的油脂。此外,金属和塑料可能随着时间的推移而变质,导致管道材料或与管道相连的部件(例如压力表、截止阀)破裂或泄漏。
6.0
微生物监测和检测偏差的调查是制药行业的关键活动,但在FDA行业指南《调查药品生产OOS (OOS)检测结果》中没有充分涵盖该领域【1】,本技术报告提供了与微生物调查相关的行业最佳实践,以消除指南中的不足。
这些调查在操作上分为两个阶段,第一阶段是实验室调查,第二阶段是生产调查,每个活动由不同的团队负责。由于微生物调查的及时性很重要,生产调查可能在实验室调查完成之前就开始了。
实验室调查的目的是确认取样和检测是正确进行的,报告的结果是有效的。调查小组通常限于进行检测的微生物学家、实验室管理人员、具有检测知识和经验的领域专家和QCU的代表。
在进行实验室调查时,应考虑以下要点:
•微生物检测中使用的样品的完整性
•进行测试的微生物学家的教育背景、技能和经验
•与微生物学家相关的测试、环境和人员监测历史
•用于测试的设备、用品、介质、稀释剂和试剂的适用性
•环境控制,包括微生物检测设施,层流罩,隔离器,和与测试相关的PPE
•培养皿菌落数读取,微生物肉汤培养基浑浊确认,数据记录,计算准确性,审查和报告结果
•
一旦微生物检测的有效性得到确认,就会组建一个多学科团队进行与失败相关的生产调查。微生物实验室、制造、工程、维护和工艺验证的代表可以是通常由QCU领导的生产调查小组的成员。为了增加成功调查的机会,通常会增加一个熟悉生产操作的有经验的制药微生物学家作为领域专家。
在生产调查中需要考虑的主要问题是:
·设备内部与故障直接相关的单元操作和位置
·周边支持区域的可能贡献
•可能导致环境控制偏差的原因,如空间压差、气流模式、温度、湿度、断电、物料转运、设施清洁和卫生
•药用原料、制药用水、中间品、包装组件和公用设施的可能贡献
·记录在批记录中的关键生产步骤的偏差,
•最近的变更控制
•相关的中控中生物负荷,环境和人员监测偏差
•与操作工、实验室管理人员和生产经理面谈,了解可能的故障原因
•跟踪微生物监测和检测
调查报告必须充分记录小组的调查结果。如果不能确定微生物检测结果超标或超标的根本原因,则必须提出最可能的原因。在结果成为不符合标准的结果之前,调查不符合趋势的结果可以帮助识别实验室和/或生产问题。为了防止这些微生物失效的再次发生,必须实施CAPA计划,由负责人员向QCU及其管理层汇报计划的进展。
7.参考文献,我就略了,应为都标好了,数字对数字应该都会。
末了:
本系列内容仅代表个人目前的知识层次和理解,
具体应用或参考请依据原文,
且本人不为此系列分享承担任何责任。
但可以友好交流讨论。
本节最后一个图是3列,所以截图上来了,不附文字,毕竟哪些微生物我没见过几个。
本系列感谢 杋稞和张功臣老师的帮助。@杋稞 @张功臣
也感谢那个审稿的家伙把我放出来,6我也加图了,嘻嘻。
本系列结束了,下个月玩点别的,比较少,就不申请专题了。

