为了使疫苗上市许可持有人《中华人民共和国疫苗管理法》《药品生产质量管理规范》《生物制品》和《药品生产监督管理办法》开展信息化转型率先实现生产、检验信息的电子数据转化
解读过程:
1.熟读上位法规指南:《中华人民共和国疫苗管理法》《药品生产质量管理规范》《生物制品》《药品生产监督管理办法》
对于如何实现“疫苗生产、检验信息的电子数据转化原则和方向
参考国家药监局-图解政策:《疫苗管理法》你问我答(三( 图解政策:《疫苗管理法》你问我答(三)
图解政策:《疫苗管理法》你问我答(三)
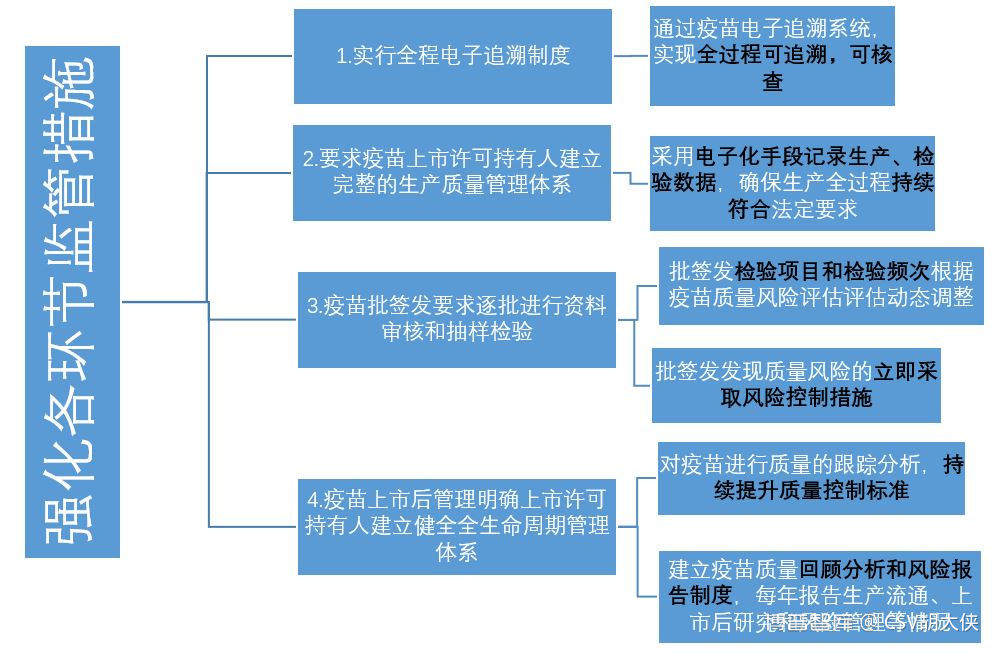
上述要点中,和CSV&DI强相关,需要GxP信息化系统与CSV验证手段的
1.1 通过疫苗电子追溯系统,实现全过程可追溯,可核查
详细信息可参考胡大侠之前文章《药品追溯码与药械UDI( 药品追溯码与药械UDI)
药品追溯码与药械UDI)

关键技术指标与业务要求:疫苗MAH国家统一字段级要求未来对接全国或者地方级追溯到最小包装
1.2 采用电子化手段记录生产、检验数据,确保生产全过程持续符合法定要求
详细信息可参考胡大侠之前文章《智慧监管-药企药监共建信息化系统的发展趋势( 智慧监管-药企药监共建信息化系统的发展趋势)
智慧监管-药企药监共建信息化系统的发展趋势)
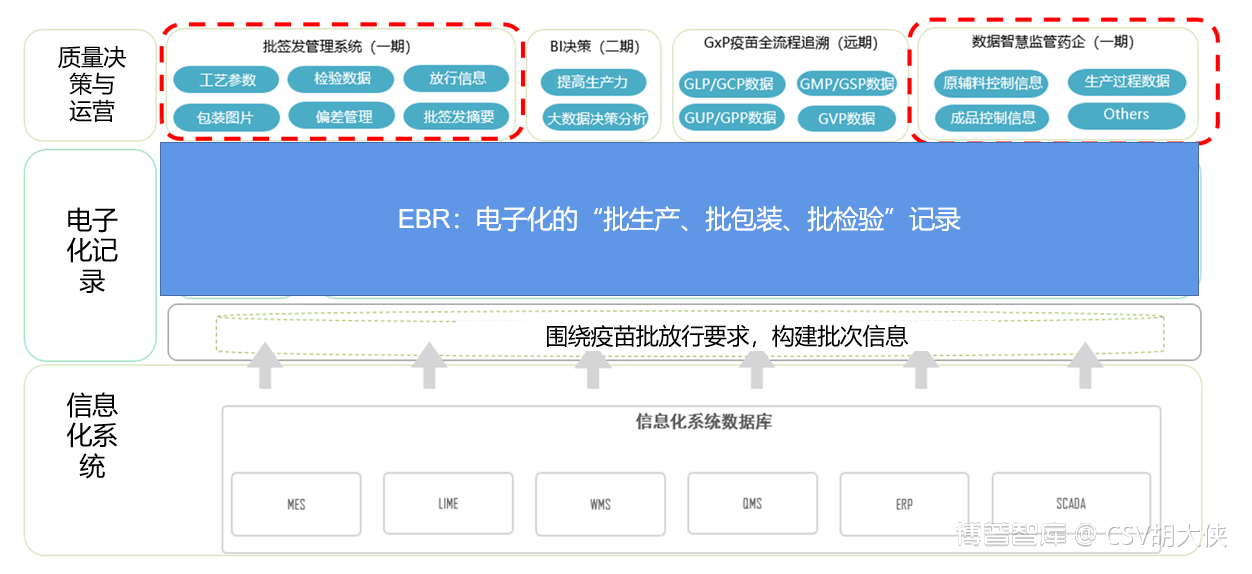
关键技术指标与业务要求:完整的生产质量管理体系【From 原料 to 成品;物料的追踪追溯&质量状态管理】- WMS+MES+LIMS采用信息化手段记录【人工纸质记录->人工键盘输入->自动采集自动记录】-(MES+LIMS)连 SCADA ELN生产、检验过程的所有数据【批生产、批包装、批检验】--(MES+LIMS)的 EBR全程持续符合【CSV系统功能权限控制,配方管理,审计追踪等】 - CSV验证

