2021年7月1日 PIC/S(国际药品认证合作组织)正式发布了 PIC/S Guidance PI 041-1 《受监管GMP/GDP环境下的数据管理和完整性良好实践》,CSV胡大侠对此进行了系列解读:
1.为什么PIC/S认为DI数据可靠性对于现场检查极其重要
PIC/S PI指南简介
国际药品检查组织( PIC/S) 是国际药品检查领域权威的机构,PIC/S 的检查标准已经成为国际药品生产管理规范( GMP) 检查的金标准和国际通行准则,国际上部分国家间基于PIC/S 检查标准达成了检查互认协议( MRAs)。相较于指导行业规范的PE前缀PI 检查官培训和现场检查的内部手册
本指南亮点解读【章节5.1- Data Governance】
1.药企数据可靠性管理机制 – 数据治理 Data Governance的必要性:

PIC/S建议,药企需形成自己的数据治理体系(Data Governance System)来为企业内GxP业务的数据可靠性提供质量保障;尽管没有法规强制要求建立一套“DataGovernance System”,但是这套体系能帮助企业在具体业务中国来定义,分级及交流数据可靠性风险,而缺失这套系统,会被(监管)认为缺少全面的数据可靠性管理系统,进而在风险管理存在不足。
关于DataGovernance System数据治理体系如何建立,在之前《“Foundation of DI by Design”-ISPE新指南 数据可靠性源自设计 品鉴1
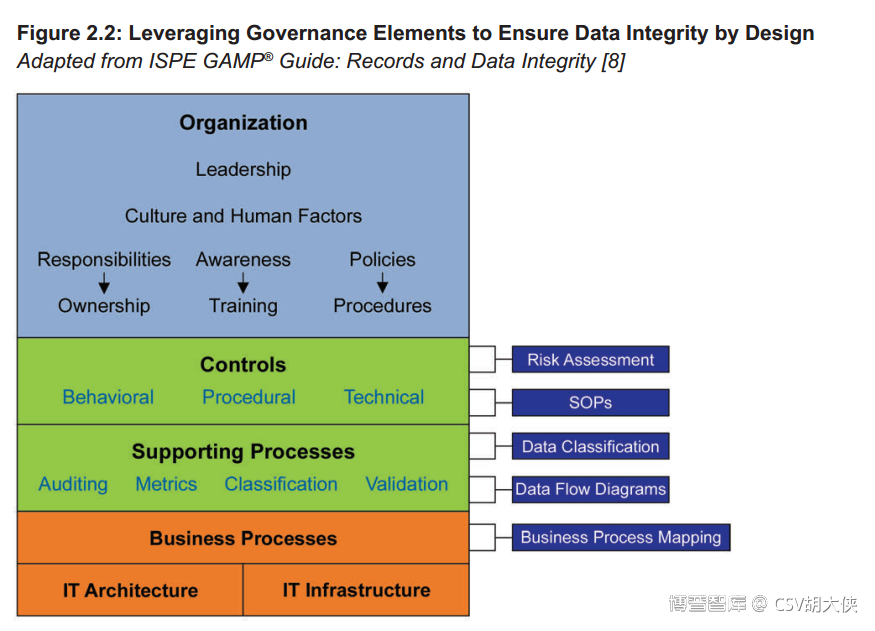
Data Governance Framework质量文化qualityculture人为因素human factors
2.药企数据治理体系的定义与作用
PIC/S建议药企针对数据治理体系的建议,需依次考虑以下几个问题
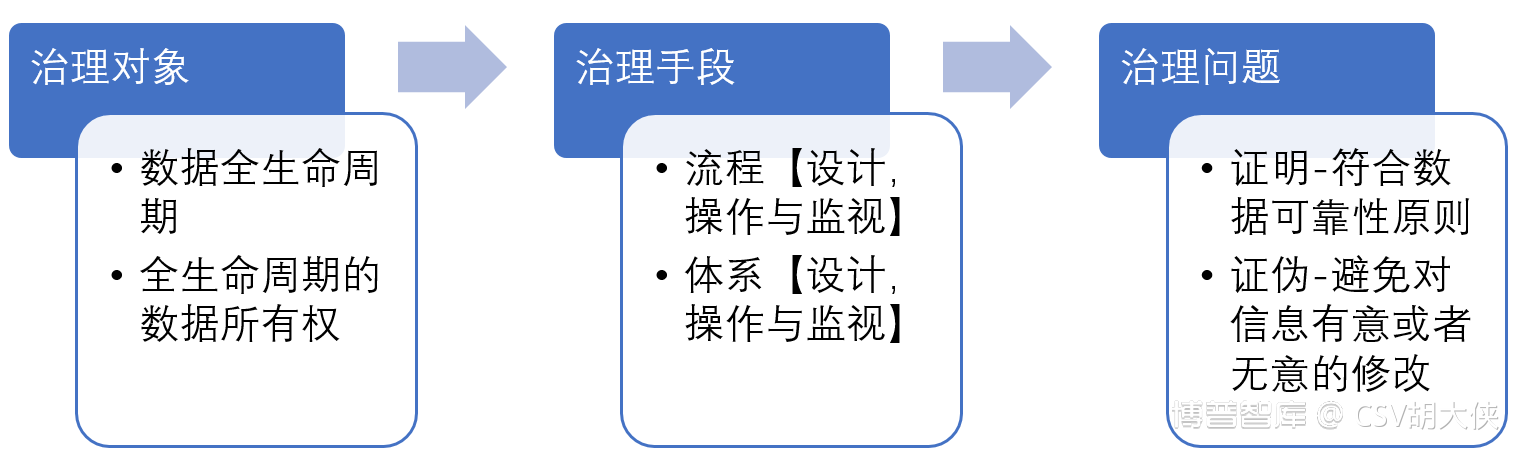
关于“数据全生命周期 – Data Life Cycle”的定义和理解:

【From - GoodPractices For Data Management And Integrity In Regulated GMP/GDP Environments20210701
关于“数据所有权 – Data Owner”的定义和理解:
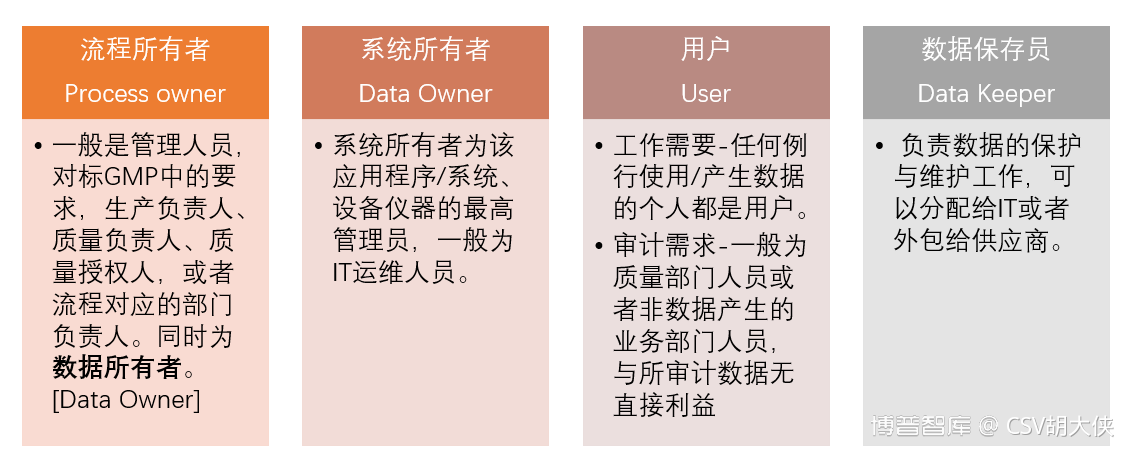
From – ISPE GAMP5 O12 SystemAdministration RBAC Role based approach control
治理(数据可靠性)手段
1.业务流程上考虑:重点是业务流程的梳理数据流的构建“Business Process Mapping” - ISPE新指南数据可靠性源于设计 品鉴5集体可视化(CollectiveVisualization)
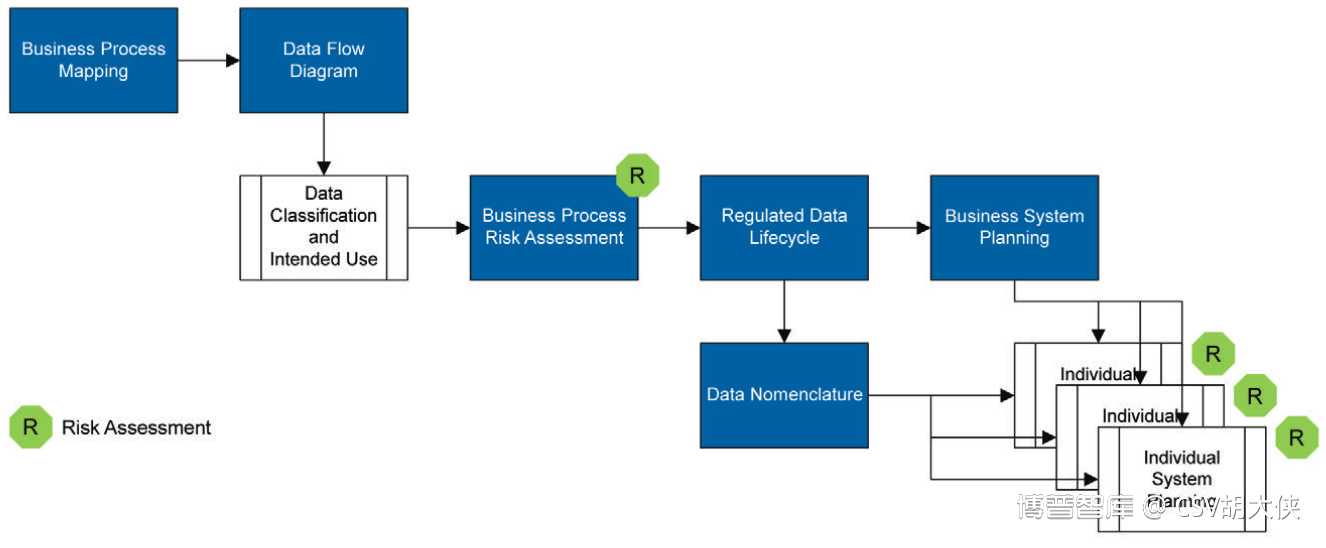
2.体系管理上考虑:双管齐下,不仅有基于人的-Organization组织管理措施;同时也有基于系统功能的-technical 技术控制措施;对于计算机化系统的数据可靠性管理,完全相信用户的自觉完全依赖系统的功能系统控制措施与质量风险管理相

【From - Good Practices For Data Management And Integrity In Regulated GMP/GDP Environments20210701
治理(数据可靠性)目的
1.通过在企业中建立数据治理体系,来向PIC/S检查员证明其所检查记录与数据的数据可靠性

图3. FDA Data Integrity 原则,引用自https://iternity.com/en/ensuring-data-integrity-in-the-long-term
2.通过在企业中建立数据治理体系,来向PIC/S检查员证伪其所检查记录与数据的真实性,而非被人为有意识篡改或者无意识的修改:
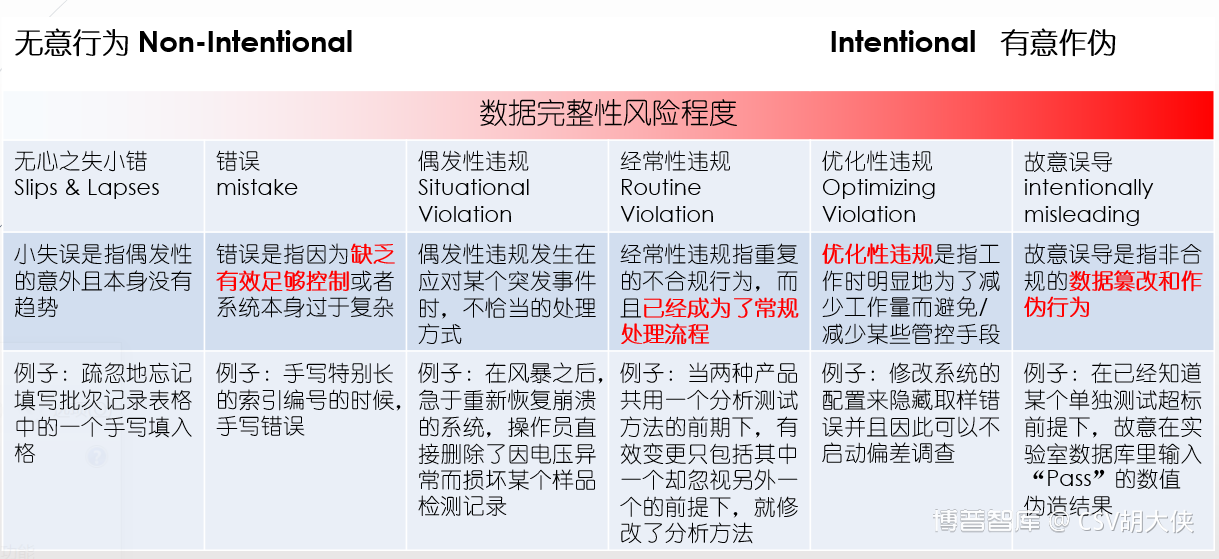
图4. ISPE Guideline Record & Data Integrity – human factor数据可靠性风险管理中人为因素的影响 参考链接
未完再续

