一、手把手教你时时看法规
身边没电脑、每天一个网站一个网站找法规汇报麻烦,这里几步教你如何快速浏览全国各省一天最新法规。
第一步:下载手机APP博谱智库

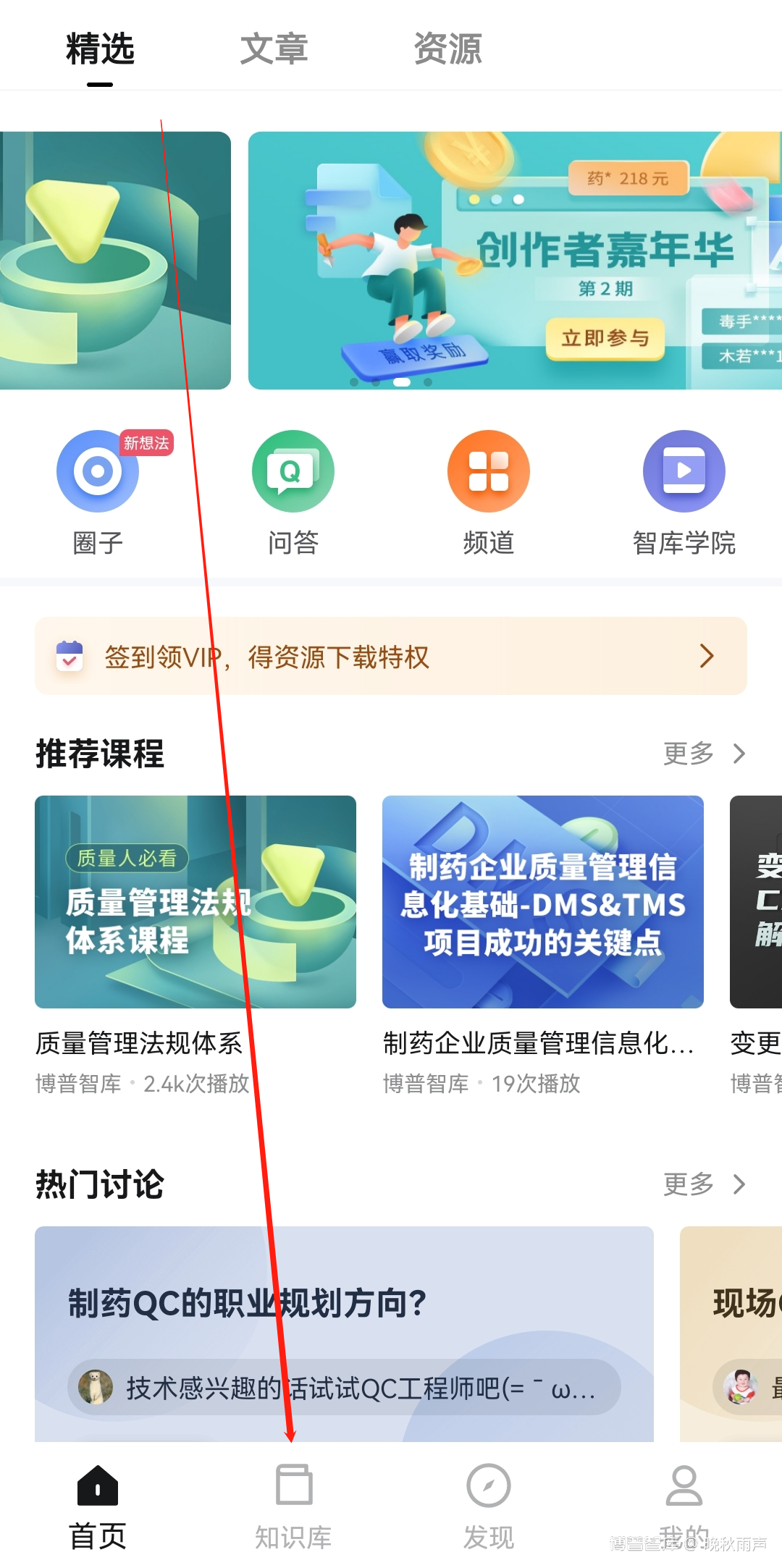
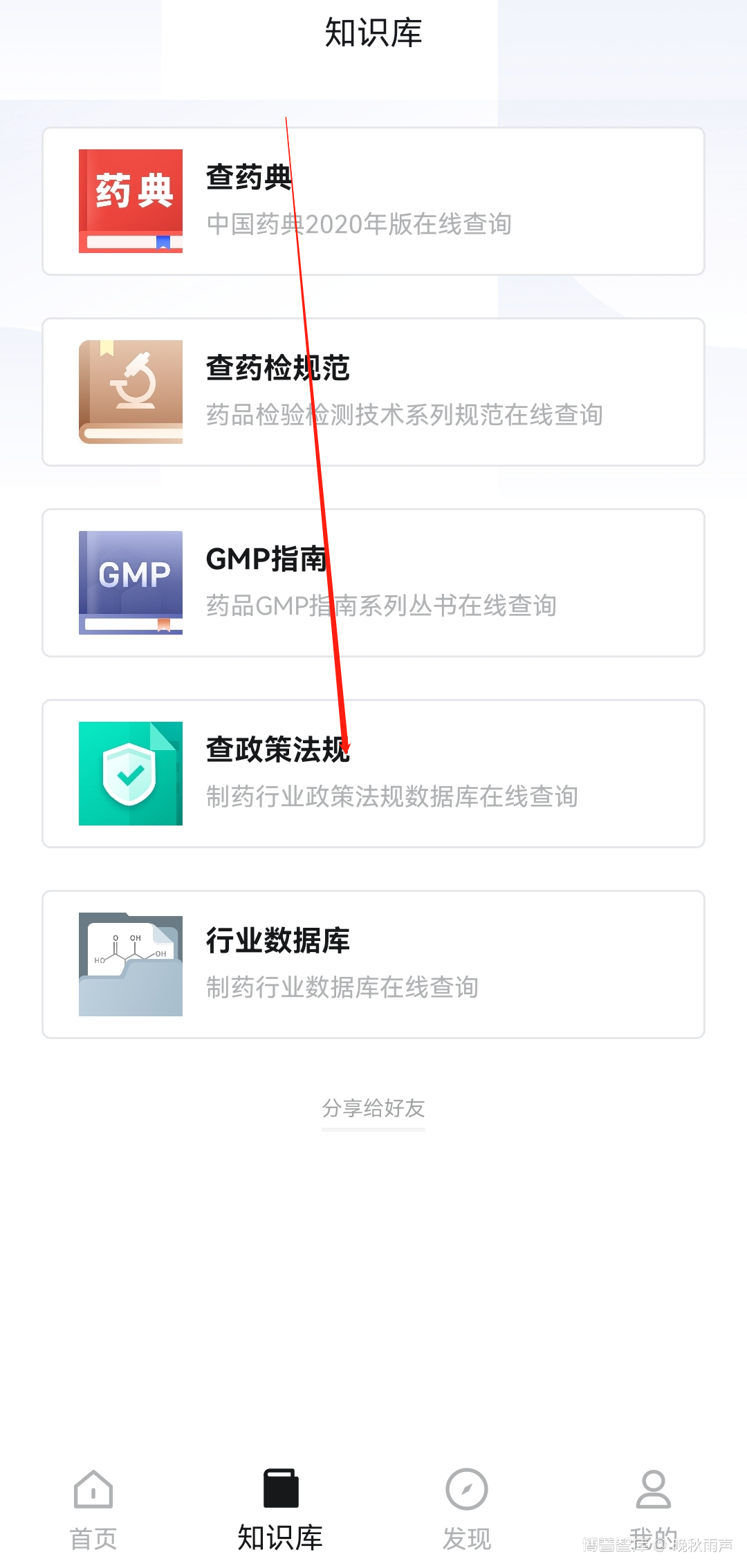
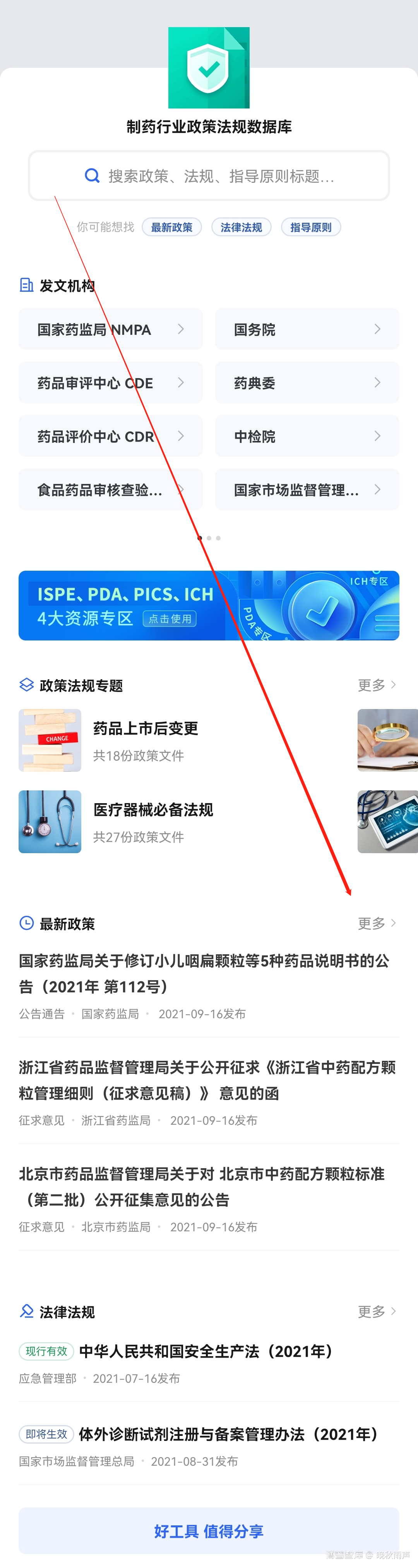
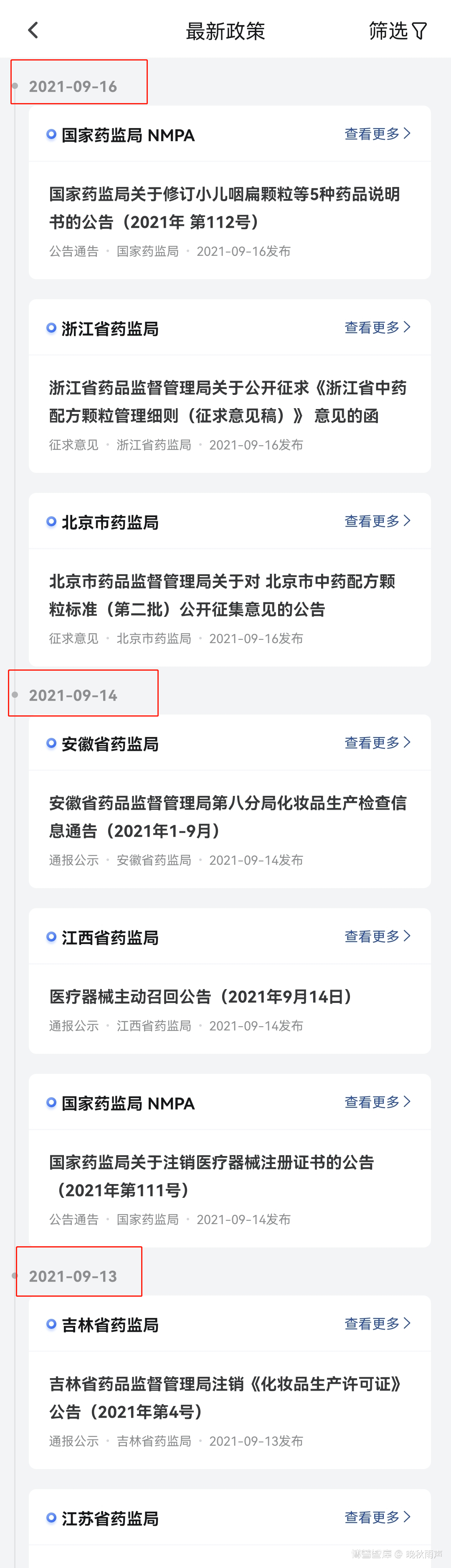
二、本周最新法规
药品
本周摘要:本周主要内容有修订说明书、中药配方颗粒管理细则(征求意见稿)、中药配方颗粒标准(征求意见稿)、国家局行政受理服务中秋国庆节假日安排、核查中心(CFDI)举办疫苗检查员和派驻检查员专题培训以及指导原则征求意见稿。
1、最近中药配方颗粒一直备受大家关注,而且各省相关管理细则和执行标准都在持续不断更新。本周浙江、北京在同日分别发布了中药配方颗粒的管理细则(征求意见稿)和执行标准(征求意见稿)。
浙江发布的中药配方管理细则(征求意见稿)适用于中药配方颗粒的备案、生产、销售、配送、使用、医保支付及其监管。本次征求意见结束时间为2021年10月3日,感兴趣的朋友可以点击文章最后的链接进行查阅。
北京发布的中药配方颗粒标准(征求意见稿)共涉及36个品种,此次为第二批发布,征求意见截止日期为2021年09月24日,这真的是留给大家的时间不多了。具体涉及的品种如下图所示:
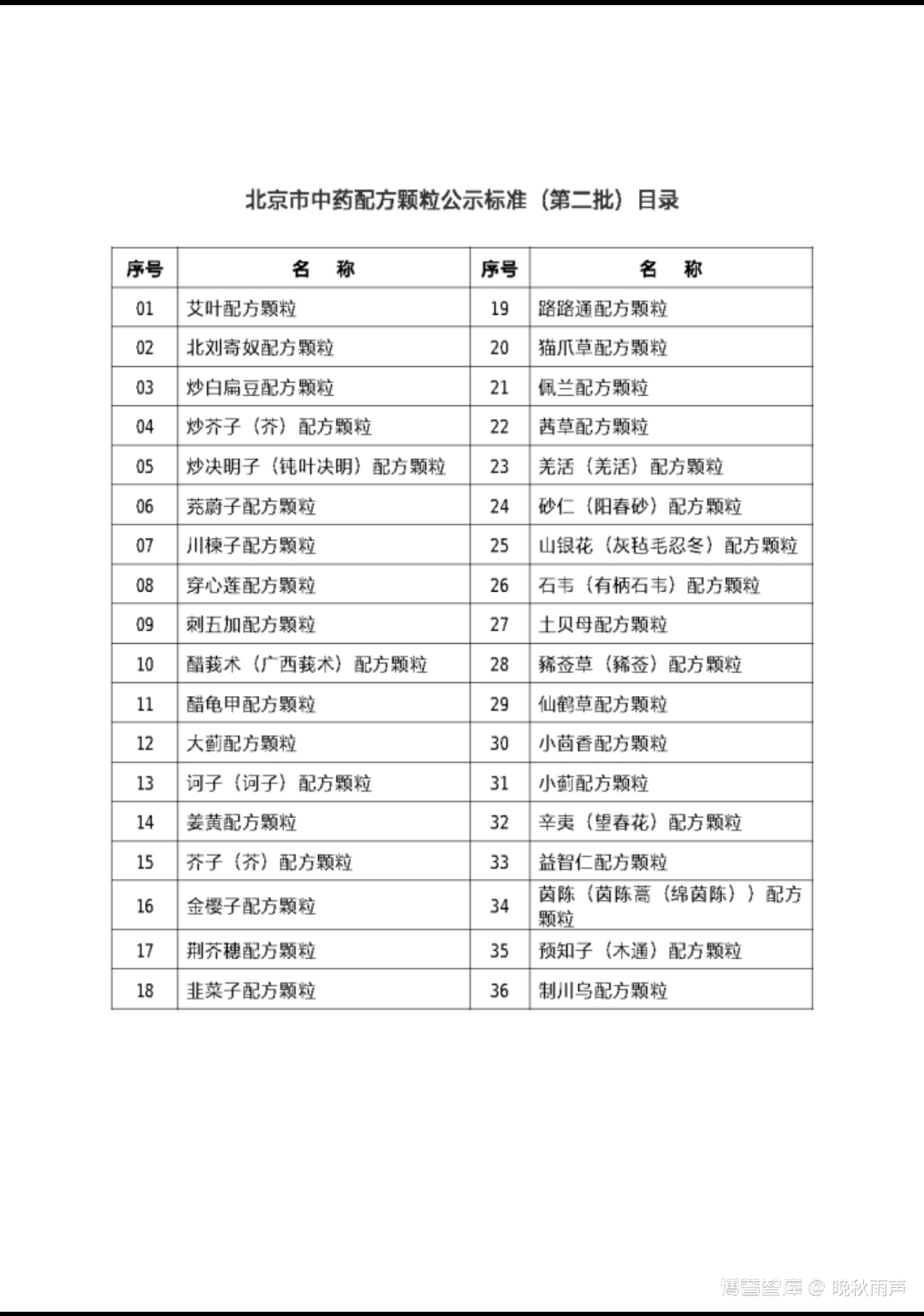
2、另外国家局也发布了5个儿童用药的药品说明书的修订公告,各持有人应当与2021年12月13日前报省级药品监督管理部门备案,备案后9个月内对已出厂的药品说明书及标签予以更换。具体品种有小儿咽扁颗粒、三黄片(胶囊)、脉血康制剂、小儿肺热咳喘制剂、舒筋活血片(胶囊),请相关企业重点关注,具体修订内容见文章最后链接。
3、国家局行政受理服务大厅2021年9月19日至21日中秋放假调休,共3天。其中9月18日(星期六)和9月20日(星期一)调休,全天对外受理、安排金库药品、GCP、GLP、麻醉药品和精神药品进出口受理电话咨询。
10月1日至7日国庆节放假调休,共7天。9月26日(星期日)和10月6日(星期三)调休,上半天对外受理,安排医疗器械受理电话咨询。10月9日(星期六)和10月7日(星期四)调休,全天对外受理,安排医疗器械、化妆品受理电话咨询。
4、2021年9月10日,世界卫生组织疫苗检查专家Ian Richard Thrussell先生,对生物制品生产企业GMP检查和审计经验进行授课。
Ian先生就近三年来对国内生物制品企业检查和审计中发现企业存在的共性问题进行了分享,主要就偏差调查、变更控制、无菌区域空调净化的设计、一次性系统、灭菌柜装载方式等方面的问题进行了全面分析;同时,通过具体的案例,对缺陷出现的原因进行深刻的剖析,并提出了有针对性的建议。就检查中遇到的实际问题,Ian先生与检查员进行了交流讨论。本次培训内容丰富,紧贴检查工作实际,为检查员现场检查能力的提升提供了有力的支持。
本次培训采用线上线下同步进行的方式,核查中心及北京市药监局的疫苗检查员和派驻检查员在现场参会,疫苗生产企业所在16个省的国家级、省级的疫苗检查员和派驻检查员以及从事疫苗监管的工作人员采用线上方式参与,共计520余名疫苗相关检查人员参加此次培训。
5、本周指导原则征求意见稿是关于嵌合抗原受体T细胞(CAR-T)产品申报上市临床风险管理计划,嵌合抗原受体T细胞治疗产品具有新颖性、复杂性和技术特异性的特点,随着此类产品的研发进展和陆续申报上市,对促进企业及早发现此类产品的风险,提供有效风险最小措施,确保上市后安全性风险可控,有必要对申报上市的临床风险管理计划提出要求和提供指导。
本指导原则共包括六个部分:概述、主要内容、安全性说明、药物警戒活动、风险最小化措施、参考文献。其中安全性说明包括一般考虑和CAR-T细胞治疗产品可能存在的安全性风险;药物警戒活动包括常规药物警戒活动和特殊药物警戒活动;风险最小化措施包括常规和额外风险最小化措施。
器械
本周摘要:本周主要内容有召回、注销医疗器械注册证书、国家药监局 国家卫生健康委 国家医保局公布了第二批实施医疗器械唯一标识工作的品种、实施时间和有关要求。
1、本周共发生两起起召回事件。
2021年09月13日江苏省发布常州市回春医疗器械有限公司生产的一次性使用输血器带针产品出现漏液,进行主动召回,等级为三级召回。赛默飞世尔(苏州)仪器有限公司生产的生物安全柜在产品标签上遗漏生产许可证编号,现主动召回,召回级别为三级。
2、北京现代高达生物技术有限责任公司共有22产品的医疗器械注册证书进行注销,具体内容见下图:
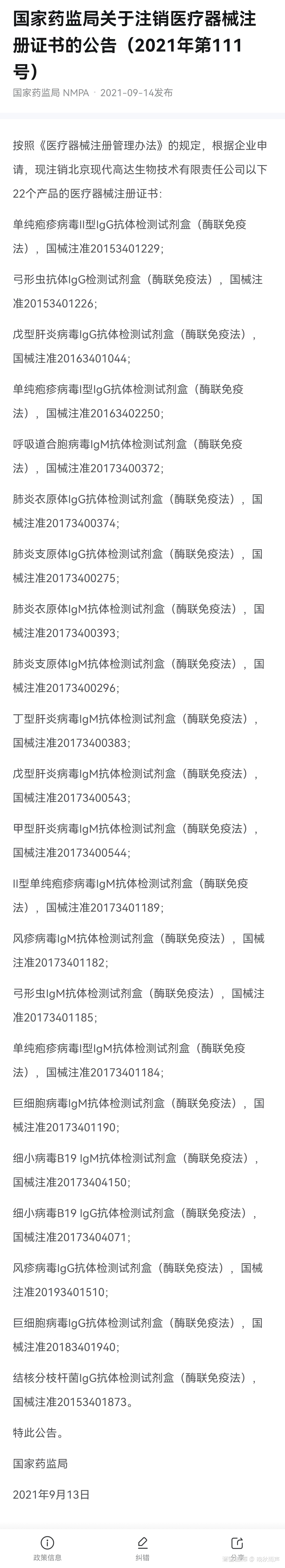
实施品种:在第一批规定的9大类69个品种的基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围,并支持和鼓励其他医疗器械品种实施唯一标识。
从2022年6月1日起,唯一标识赋码、唯一标识注册系统提交、唯一标识数据库提交将正式实施
三、一周法规链接
药品
1、国家药监局关于修订小儿咽扁颗粒等5种药品说明书的公告(2021年 第112号)( 国家药监局关于修订小儿咽扁颗粒等5种药品说明书的公告(2021年 第112号))
国家药监局关于修订小儿咽扁颗粒等5种药品说明书的公告(2021年 第112号))
2、浙江省药品监督管理局关于公开征求《浙江省中药配方颗粒管理细则(征求意见稿)》 意见的函( 浙江省药品监督管理局关于公开征求《浙江省中药配方颗粒管理细则(征求意见稿)》 意见的函)
浙江省药品监督管理局关于公开征求《浙江省中药配方颗粒管理细则(征求意见稿)》 意见的函)
3、北京市药品监督管理局关于对 北京市中药配方颗粒标准(第二批)公开征集意见的公告( 北京市药品监督管理局关于对 北京市中药配方颗粒标准(第二批)公开征集意见的公告)
北京市药品监督管理局关于对 北京市中药配方颗粒标准(第二批)公开征集意见的公告)
4、国家药品监督管理局行政受理服务大厅关于2021年中秋节、国庆节放假安排的公告(第292号)( 国家药品监督管理局行政受理服务大厅关于2021年中秋节、国庆节放假安排的公告(第292号))
国家药品监督管理局行政受理服务大厅关于2021年中秋节、国庆节放假安排的公告(第292号))
5、核查中心举办2021年疫苗检查员和派驻检查员专题培训( 核查中心举办2021年疫苗检查员和派驻检查员专题培训)
核查中心举办2021年疫苗检查员和派驻检查员专题培训)
6、关于公开征求《嵌合抗原受体T细胞(CAR-T)产品申报上市临床风险管理计划技术指导原则(征求意见稿)》意见的通知( 关于公开征求《嵌合抗原受体T细胞(CAR-T)产品申报上市临床风险管理计划技术指导原则(征求意见稿)》意见的通知)
关于公开征求《嵌合抗原受体T细胞(CAR-T)产品申报上市临床风险管理计划技术指导原则(征求意见稿)》意见的通知)
器械
1、国家药监局关于注销医疗器械注册证书的公告(2021年第111号)( 国家药监局关于注销医疗器械注册证书的公告(2021年第111号))
国家药监局关于注销医疗器械注册证书的公告(2021年第111号))
2、常州市回春医疗器材有限公司对一次性使用输血器带针主动召回( 常州市回春医疗器材有限公司对一次性使用输血器带针主动召回)
常州市回春医疗器材有限公司对一次性使用输血器带针主动召回)
3、赛默飞世尔(苏州)仪器有限公司对生物安全柜主动召回( 赛默飞世尔(苏州)仪器有限公司对生物安全柜主动召回)
赛默飞世尔(苏州)仪器有限公司对生物安全柜主动召回)
4、国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告(2021年第114号 )( 国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告(2021年第114号 ))
国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告(2021年第114号 ))

