7月20日一早,我醒来,按照终年不改的陋习,打开朋友圈,满屏皆是这可是颠覆性重磅消息啊!脑子里回旋的全是
通知清清楚楚点名该指南的目的
按照长年习得的良好作风,对任何一件新法律法规,都要通读,从中掌握政策动向,明晰最新要求,进而自我反省,查漏补缺,紧跟业态发展。学习完之后,结合最初该指南刷爆朋友圈,但是昙花一现,近几日早已偃旗息鼓的现实,我觉得大家把她忽视了!
抛开化学药品和生物制品不说,我们摘取中药相关内容,一一道来。
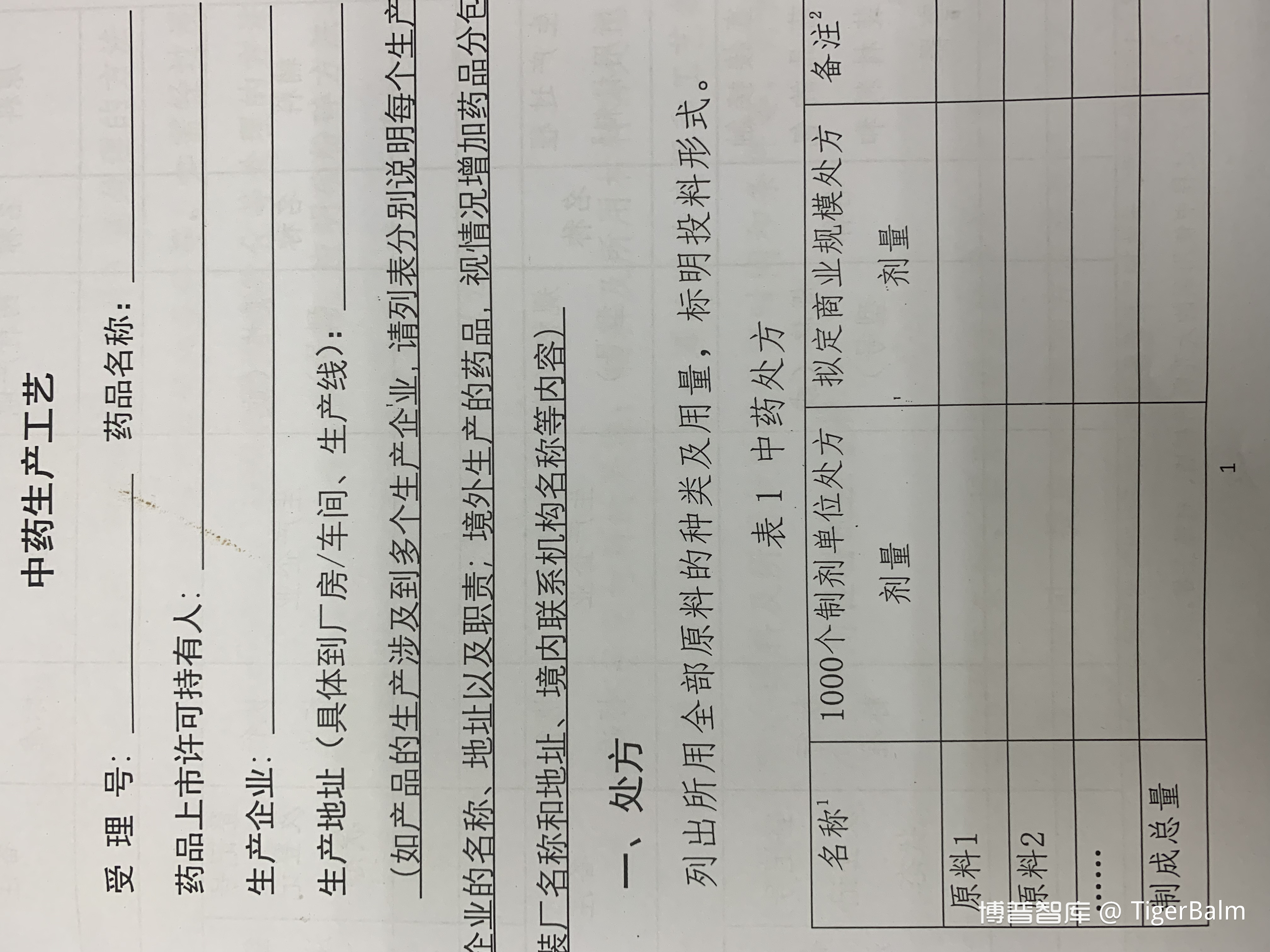
如上图所示,1、“受理号”已经亮明身份,再次表示它的使用范围。2、“拟定商业规模处方剂量”,若是生产使用工艺,肯定不会这么填表。
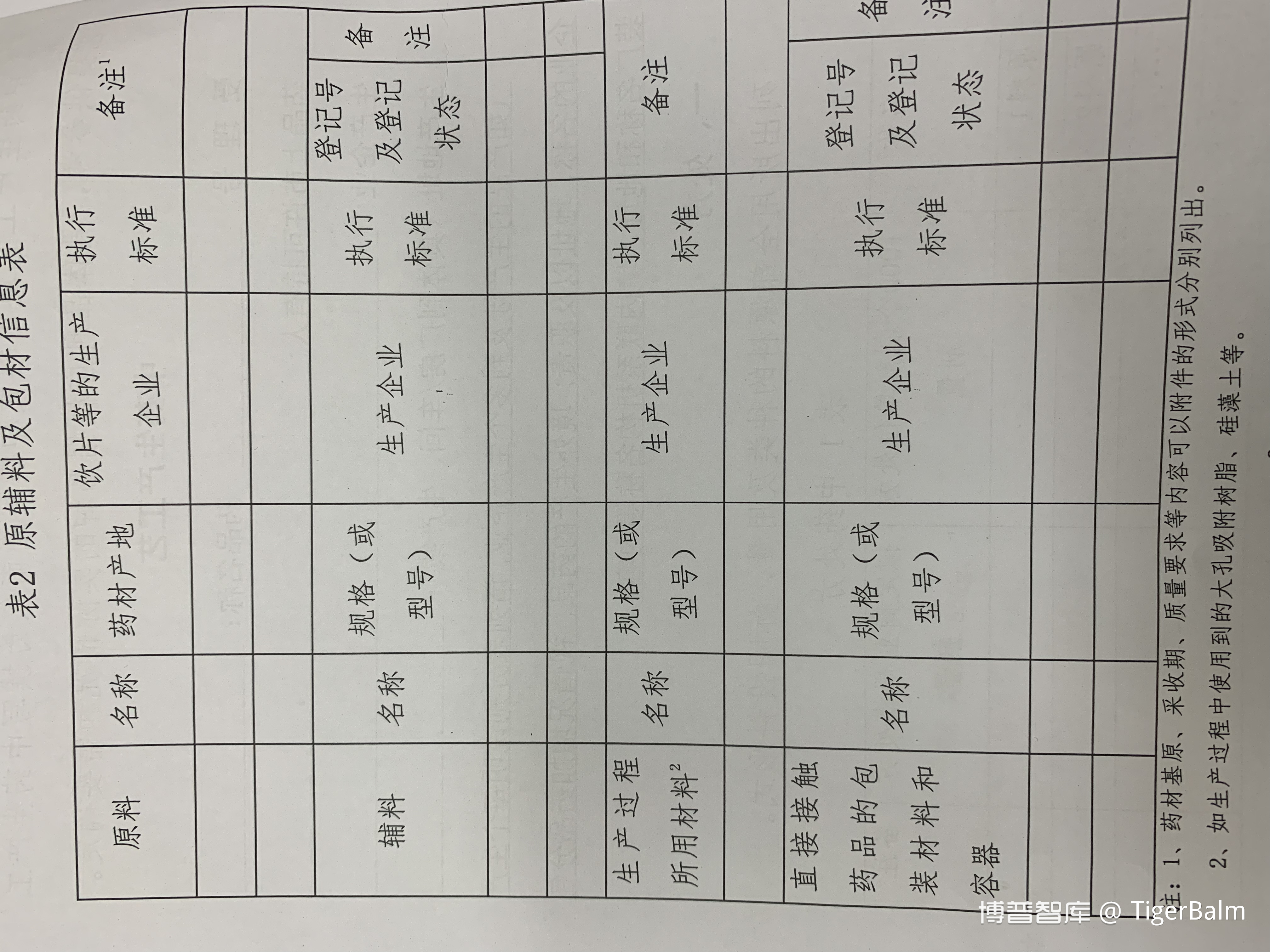
“原辅料、制备过程中所用材料、直接接触药品的包装材料”中“生产过程所用材料”在表格下方小字“注:2、如生产过程中使用到的大孔吸附树脂、硅藻土等。”对应表格中要求写明“规格(或型号)”,显然要求是非常严格的。例如、中药生产中必须用到的过滤材料,如滤布,细分材质和型号非常多,其对药液质量是有影响的,这是常识,但是究竟如何影响,影响程度多大,不得而知。一直以来中药标准很多较粗放,众多标准还没有含量等要求,随着标准的不断提升,难免出现不再合格的情况。企业如果缺乏对此深入研究,现在依葫芦画瓢报上去,未来可能出现“出来混,迟早是要还”的囧境。
继续往后面学习,到了具体的1)原料的前处理:……切制规格等;需粉碎后投料的,应明确粉碎方法、粒径或粒度等;需破碎的应明确破碎方法、破碎后药材大小等;……”二、“3.提取……提取温度、时间,提取液过滤的方法及条件,……”三、“4.浓缩 明确浓缩的方法、条件,如温度、压力、时间……明确浓缩液的相对密度或浓缩液重量(体积)与饮片的比例,明确浓缩液或浸膏的得率范围。”甚至于,“如滤材阻塞、损坏时更换滤材或维修处理的相关指标、方法及要求。”
以上图示及举例已经说明此文件内容和宗旨,其它不再一一陈述。
请注意,这份看似轻描淡写的指南,想到它用于

