清洁的过程要有效去除上批产品的残留,主要是有效成分的残留。如果活性成分易降解,还要考虑降解产物残留。清洁过程使用的清洁剂最好是水。如果使用其它清洁剂,如酸液、碱液、表面活性剂、有机试剂等,还要将这些清洁剂去除。需要注意的是,有机溶剂的选择必须选择ICH Q3C中规定的3类溶剂。其他类溶剂因毒性较大,不允许用作清洁剂。表面活性剂要选择成分明确的产品,不能选择洗洁精等家用清洁剂。对于微生物有要求的产品,清洁残留也要考虑微生物限度。当然,也有专家认为,微生物的控制属于消毒灭菌过程,不算在清洁之中;笔者认为,这种说法也有一定的科学性,但清洁验证中大多数情况是不加以区分的。尤其是原料药和口服固体制剂。因此,清洁验证中的残留一般包括活性残留,清洁剂残留和微生物残留。
清洁过程是不可能将已使用的设备清洁至完全无残留的状态。既然有残留,那残留限度该如何制定才能确保患者安全和产品不被污染呢?下面星辰就为各位读者介绍制定残留限度标准的方法。
1.活性残留
在星辰的前篇文章《星辰经验谈:如何制定清洁验证方案》中,我给大家简单介绍了三个计算活性残留的公式,下面将对这几个公式进行展开解释。
1)默认限度:一般选择10ppm,计算公式如下:
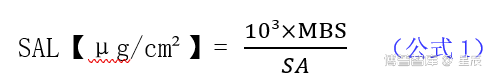
将残留物限度定为10ppm(即10×10-6)多为发达国家生产液体制剂,如溶液、乳剂等剂型的企业采用。一般来说,除非是高活性、高致敏性的药品,该限度是足够安全的。该10ppm标准也适用于固体制剂。对于原料药来说,该标准可定为5-500ppm(原料药中100ppm是很常见的)。通用限度应该有科学理由支持并有书面记录。
2)基于日剂量
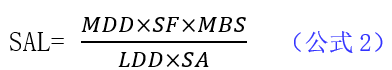
MDD为已清洁产品的最小日剂量,TDD为拟下次生产产品的最大日剂量。
目前对于MDD的选择有两种观点,第一种是MDD为目标产品的最小日剂量,另一种观点是为使ARL得到最小值,MDD应选择共线生产产品中最小的,即不一定非要选择目标产品的MDD。这两种观点目前并存,都有道理,各位读者可根据自己公司实际情况来选择。
此计算公式的使用还有三点需要注意:1. 对于制剂产品来说,MDD是前一产品即目标产品的API的最小日治疗剂量,TDD是后一产品API+辅料的量,即制剂的最大日剂量。2.对于原料药,MDD和TDD均为API的量。3.如果两种产品的给药频率不同,需要做相应的调整,使之在同一水平上。比如A产品(目标产品)为每日给药1次,B产品(拟下一生产产品)每周给药1次,则需要将A产品日剂量×7,或B产品TDD÷7。
3)基于毒性
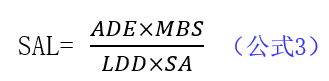
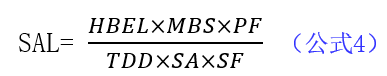
此公式中,HBEL中文意思为基于健康的暴露限值,TDD与上面公式中LDD相同,为拟后一生产产品最大日治疗剂量,PF为清除因子,反映一个工艺降低之前水平在下一物料的下游合成路线中水平的能力(如果下一物料并非最终API),默认值为“1”则默认值为“1”。
由上面公式可以看出,计算残留限度,必须得到HBEL值,HBEL表示为可接受的日暴露值(ADE)或允许日暴露值(PDE)。

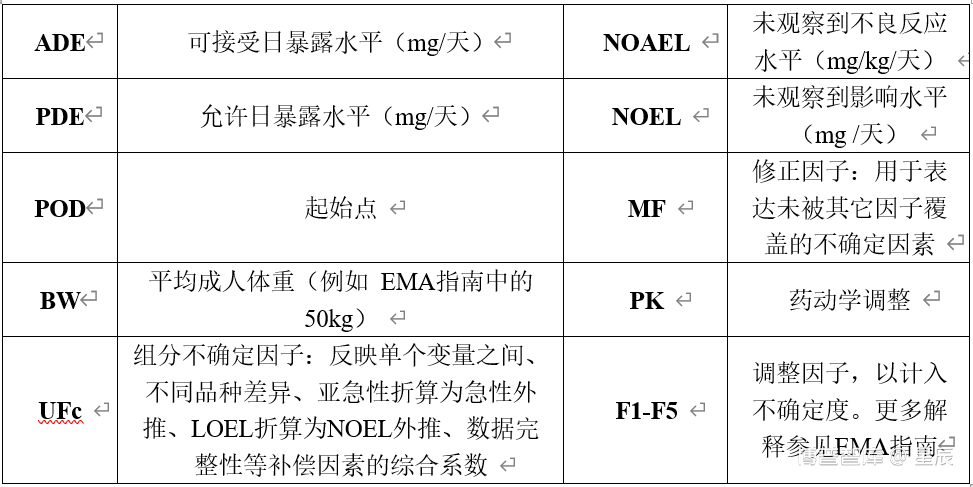
HBEL(ADE/PDE)的获得有几种途径,首先是有现成的数据,可以直接使用;二是通过上述公式计算得到,式中POD(起始点)应优先使用NOAEL/NOEL,如果实在查不到,可以使用LD50(半数致死量)进行计算。但是这种情况下需要采用保守方法,因此需要使用更多不确定因子。
LD50计算NOEL的公式为:
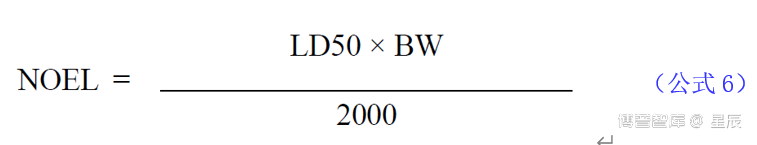
2.清洁剂残留限度
对于大多数溶剂和清洁剂来说,HBEL已经过了计算,在公共数据库中可以获得:ACGIH、OSHA、MAH、NIOSH等,可直接带入公式4
3. 微生物残留限度
对于微生物残留限度,建议D级洁净区设备为2cfu/cm²,C级洁净区设备为1cfu/cm²。

